Электрохимическая кинетика
Cтраница 3
Согласно законам электрохимической кинетики, скорость анодного растворения металла должна возрастать при увеличении потенциала электрода. [31]
Согласно законам электрохимической кинетики, скорость протекающего на электроде процесса связана экспоненциальной функцией с иотенциалом и не зависит от наличия других, одновременно протекающих процессов, при постоянной концентрации реагирующих веществ. [32]
На развитии электрохимической кинетики в течение ряда лет неблагоприятно сказывалось влияние представления, согласно которому наблюдаемая скорость электрохимической реакции, как правило, определяется не скоростью элементарного акта присоединения или отщепления электронов, а протеканием вторичных химических превращений. Предполагалось, что таковыми в случае процессов электровосстановления и электроокисления являются реакции, соответственно, с участием атомов водорода и кислорода, к случае разряда иона водорода-реакция рекомбинации атомов в молекулу или другая реакция, приводящая к удалению адсорбированного атома водорода с поверхности электрода. [33]
Основные закономерности электрохимической кинетики, установленные для водных растворов, справедливы и в отношении ионных расплавов. Вместе с тем эти закономерности характеризуются некоторыми особенностями. [34]
Теоретические представления электрохимической кинетики в настоящее время широко применяются к самым разнообразным электродным реакциям, причем не только к реакциям разряда отдельных ионов, но и к более сложным процессам, включающим одновременно и разряд, и химическую реакцию. [35]
Специфической областью электрохимической кинетики является раздел, посвященный электрокристаллизации. Теория электрокристаллизации имеет большое значение для таких важных приложений электрохимии, как электрометаллургия и, особенно, гальванотехника. Процесс электрокристаллизации связан с образованием на поверхности электрода зародыша новой фазы и последующим ростом его. [36]
Теоретические представления электрохимической кинетики в настоящее время широко применяются к самым разнообразным электродным реакциям, причем не только к реакциям разряда отдельных ионов, но и к более сложным процессам, включающим одновременно и разряд, и химическую реакцию. [37]
Специфической областью электрохимической кинетики является раздел, посвященный электрокристаллизации. Теория электрокристаллизации имеет большое значение для таких важных приложений электрохимии, как электрометаллургия и, особенно, гальванотехника. Процесс электрокристаллизации связан с образованием на поверхности электрода зародыша новой фазы и последующим ростом его. [38]
Консолидации основ электрохимической кинетики способствовало распространение кинетических исследований на значительно более широкий круг электрохимических процессов. Так, в последние годы были изучены кинетика обмена между амальгамами и ионами металлов, реакции восстановления ряда простых и комплексных ионов, получены, хотя и недостаточно полные, но весьма многочисленные данные по электрохимии органических соединений. Существенную роль при этом сыграло использование удобной и хорошо воспроизводимой формы электрода, каким является предложенный Гсйровским капельный ртутный электрод. [39]
Специфические черты электрохимической кинетики выступают особенно ярко при рассмотрении непосредственно электрохимической стадии процесса, протекающей в электрическом поле двойного слоя у поверхности электрода. Именно наличие этсй стадии заставляет выделить кинетику электродных процессов из общих рамок химической кинетики, придает ей в известном смысле самостоятельность. Электрическое поле двойного слоя влияет как на величину энергии активации элементарного акта разряда, так и на эффективную концентрацию реагирующих частиц. Теория эта применима и к другим электрохимическим реакциям. [40]
Согласно закону электрохимической кинетики скорость анодного растворения должна возрастать при увеличении химического потенциала, однако в рассматриваемом случае этого не происходит. Вследствие образования сервовитной пленки меди между анодными и катодными участками поверхности бронзы процесс растворения может полностью прекратиться, и тогда наступит установившийся режим трения. [41]
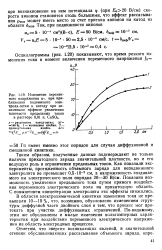 |
Изменение переменного напряжения и - при приближении подвижного электрода-сетки к катоду при неизменном эффекте увеличения плотности предельных токов в растворе 0 01 и. CuSO4. [42] |
В области электрохимической кинетики изменения тока не превышали 10 - 15 %, что, возможно, обусловлено изменением структуры диффузной части двойного слоя и тем, что процесс мог протекать при участии диффузионных ограничений. По-видимому, этим же обусловлены и малые изменения вольтамперных характеристик при воздействии переменного электрического напряжения на область электродных процессов. [43]
Интересно сочетание диффузионной и электрохимической кинетики при работе пористых электродов. Важную роль в их поведении играют омическое сопротивление раствора, заполняющего поры, и, в некоторых случаях, сопротивление металлической матрицы. [44]
При изучении электрохимической кинетики перезарядки ионов обратимых систем в растворе нами была обнаружена интересная закономерность. [45]
Страницы: 1 2 3 4