Истинная кинетика - реакция
Cтраница 1
Истинная кинетика реакции характеризуется первым порядком по водороду и нулевым порядком по ацетилену и этилену. Очевидно, что если наблюдаются диффузионные ограничения в отношении ацетилена, то гидрирование будет протекать в глубине гранулы. Эксперименты Марса и Горгельса показали, что задача может быть решена различными путями, основанными на теории. К числу этих путей относятся: использование широкопористых катализаторов; нанесение палладия тонким поверхностным слоем на гранулу; работа при низких температурах. Последняя должна быть достаточно низкой для того, чтобы уменьшить скорость реакции до значения, соответствующего Т) Я. [1]
Исследование истинной кинетики реакции показало, что ее скорость пропорциональна концентрации кислорода в степени 0 8, а кажущаяся энергия активации равна 21 9 кДж / моль. Был измерен коэффициент теплопроводности катализатора, исходя из значения которого по уравнению (IV.2) вычисляли эффективный коэффициент диффузии. [2]
В случаях, когда истинная кинетика реакции не поддается определению, приходится ограничиваться нахождением псевдокинетических данных и значений температурных коэффициентов Другой более часто используемой возможностью является определение скорости реакции или какой-нибудь функции этой величины при точно заданных условиях. Влияние скрытых переменных факторов может сказаться на воспроизводимости результатов и препятствовать экстраполированию получаемых данных. [3]
На характер зависимости ц от ф влияет как истинная кинетика реакции, так и форма гранулы ( стр. [4]
Реальные кинетические закономерности гетерогенного каталитического процесса определяются как истинной кинетикой реакции на активной поверхности, так и условиями массо - и теплопереноса. Их изучение и составляет предмет макрокинетики, или так называемой диффузионной кинетики химических процессов. [5]
Следующая стадит моделирования - описание процесса на зерне катализатора с учетом истинной кинетики реакции. Применяемые на практике катализаторы синтеза аммиака являются пористыми телами с развитой внутренней поверхностью. [6]
Измерение скорости реакции в диффузионной области ничего не может сказать нам об истинной кинетике реакции и ее химическом механизме. Но зато измерение скорости реакции в диффузионной области может служить методом исследования диффузионных процессов, в частности конвективной диффузии. [7]
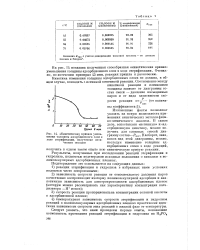 |
Кинетическая кривая уменьшения толщины адсорбционного слоя в ходе этерификации, полученная оптическим методом. [8] |
Кинетика изменения толщины адсорбционных слоев не должна, в общем случае, совпадать с истинной кинетикой реакции. [9]
Если точки ложатся на прямую линию, то считается, что предполагаемая кинетика является истинной кинетикой реакции. [10]
Если точки ложатся на прямую линию, то считается, что предполагаемая кинетика является истинной кинетикой реакции. [11]
 |
Сопоставление кинетических данных для реакций нулевого, половинного и второго порядков с кинетикой реакции первого порядка. [12] |
Если экспериментальные точки ложатся на прямую линию, то считается, что указанное уравнение передает истинную кинетику реакции. [13]
Очевидно, что тем же методом легко могут быть рассмотрены и более сложные случаи, когда истинная кинетика реакции на поверхности дисперсных частиц не удовлетворяет первому порядку. [14]
Важно установить, почему протекание обменной реакции со временем характеризуется кажущимся первым порядком, какой бы ни была истинная кинетика реакции. Недооценка этой особенности обменных реакций иногда приводит к неправильным заключениям об определяющей скорость стадии в такого рода реакциях. Целесообразно рассмотреть характерный пример - обмен этана с дейтерием. [15]
Страницы: 1 2 3