Кислород - решетка
Cтраница 1
Кислород решетки окислов металлов, а также кислород, адсорбированный на их поверхности, малоподвижен. В определенных условиях углеводород вступает в реакцию с кислородом решетки катализатора. Значение этой побочной реакции в окислительном процессе при низких температурах невелико. [1]
Подвижность кислорода решетки легко обнаружить по изотопному кислородному обмену. Результаты работ Винтера [13], Т. В. Борескова и Л. А. Касаткиной [14], Камерона и других [15], а также наши экспериментальные данные показали, что при температурах каталитического процесса на Mn02, V05, Cu. Аналогичное комплексообразование наблюдается и на металлах серебре и платине, покрытых кислородом. Исследование изотопного обмена углекислого газа, содержащего О18 или смеси С02 016018, подтверждает предположение об образовании такого комплекса на поверхности. На рис. 4 показаны диаграмма скоростей кислородного обмена с С02 на различных катализаторах и для сравнения - скорости изотопного обмена С02 при реакции этилена с тяжелым кислородом. Из этих данных следует, что скорости изотопного обмена С02 без реакции в 2 - 3 раза выше, чем в условиях окислительного процесса. [2]
Катализаторы, обладающие подвижным кислородом решетки, в отсутствие молекулярного кислорода задерживают процесс на стадии димеризации. На Bi2O3 из пропилена при 450 - 500 С образуется гексадиен-1 5 с селективностью 79 - 82 % [16]; восстановленный катализатор затем регенерируют, пропуская над ним кислородо-азотную смесь при 450 - 500 С. [3]
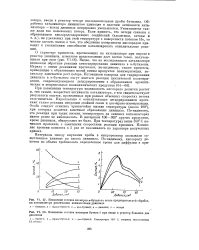 |
Изменение состава изомеров н-бутилена после предварительной обработки катализатора различными количествами дивинила.| Изменение состава изомеров бутена-1 при вводе в реактор больших доз дивинила. [4] |
При повышении температуры подвижность кислорода решетки растет и, тем самым, возрастает активность катализатора, о чем свидетельствуют результаты опытов, проведенных при разных объемных скоростях потока газа-носителя. Параллельно с окислительным дегидрированием протекают также реакции миграции двойной связи и z / uc - ягранс-изомеризации. Особо следует отметить чрезвычайно низкие температуры ( около 100), при которых делается заметным образование дивинила. [5]
Так как скорости обмена кислорода решетки и обмена на поверхности сравнимы, следует считать, что энергия связи кислород - металл важна для каталитических процессов окисления. Из окислов наиболее активны окислы переходных металлов с 3, 4, 8 и 9 d - электронами в катионах, и теплоты превращения высших окислов в низшие, например V5 - - V4 или Со3О4 - - СоО, служат хорошими ориентировочными данными для оценки каталитической активности. [6]
Небольшая доля С6Н6 окисляется кислородом решетки, но скорость этой реакции значительно меньше первой. [7]
 |
Спектры ЭСХА Мо 3d и Со /. 3 / 2 в восстановленных водородом при 400 С молибдатах кобальта. а - Мо 3d. б - Со рз /. / - а - СоМоО4. 2 - Р - СоМоО. [8] |
По данны-м [263], разные атомы кислорода решетки, участвующие в окислении, не равноценны. Селективный катализатор; должен иметь ионы кислорода, расположенные в разных кристаллографических положениях, и эти ионы должны обладать разной, энергией авязи с соседними ионами металла. [9]
Реакция образующегося иона карбония с анионом кислорода решетки оксида ванадия ведет к иону алкоголята, который затем окисляется в о-толуиловый альдегид. [10]
В образовании аллильной промежуточной формы участвует адсорбированный кислород или кислород решетки катализатора. [11]
Ото положение катиона определяет и равновесные расстояния до атомов кислорода решетки. [12]
С помощью метода изотопного обмена была выяснена важная роль кислорода решетки в процессах разложения закиси азота и окисления окиси углерода ( для более полного ознакомления с механизмом последней реакции см. гл. Кроме того, метод изотопного обмена 180, как и радиохимический метод ( разд. [13]
При исследовании реакции гетеромолекулярного обмена О18 с поверхностными атомами кислорода решетки носителя было установлено существенное влияние на эту реакцию условий предварительной тренировки катализатора, причем в восстановительной среде подвижность атомов кислорода окиси алюминия увеличилась в 2 раза. Нам кажется, что одной из причин резкого уменьшения ионной формы платины в восстановительной среде является рост подвижности ионов платины под влиянием увеличения подвижности кислородных атомов носителя. Видимо, во взаимном влиянии металла и носителя в различных условиях следует искать причину разнофазных состояний платины и, как следствие, ответа на. [14]
По механизму восстановления - окисления молекула реагента взаимодействует с кислородом решетки и восстанавливает поверхность катализатора, которая снова окисляется кислородом из газовой фазы. Для многих реакций окисления на оксидных катализаторах может быть принят механизм Марса - ван - Кревелена [35], который объясняет высокую активность оксидов металлов, легко изменяющих степень окисления. [15]
Страницы: 1 2 3 4