Кислород - решетка
Cтраница 2
Предварительные данные по изотопному обмену кислорода газовой фазы с кислородом решетки показали, что в интервале температур 350 - 550 С доля обменявшегося кислорода возрастает при переходе от окиси молибдена к окиси висмута. В обмене участвует не только кислород поверхности, но и кислород из объема решетки. Обмен на всех катализаторах изучался после их тренировки в вакууме при 450 С. [16]
В остальных же случаях в начальный период работы окисных катализаторов кислород решетки окисла может принимать участие в образовании продуктов реакции. [17]
В работах по кинетике реакций окисления углеводородов побочная реакция окисления кислородом решетки обычно не учитывалась. В 1937 г. при выводе кинетических уравнений по окислению СО на Мп02 Елович [251 ] предположил, что катализ происходит на участках свежевосстановленной поверхности МнОа, которая в момент образования обладает повышенной способностью к регенерации. Для этих вариантов механизма реакции кинетические уравнения идентичны. [18]
 |
Состояния адсорбированного кислорода на металлах. [19] |
О, - неполностью восстановленные активные формы кислорода; Ог - кислород решетки катализатора; о - вакансия в кислородной субрешетке катализатора; R - окисляемое органическое соединение; ВО - продукт селективного ( парциального) окисления. [20]
Наконец, учитывая отсутствие водородных: вязей между NH3 и атомами кислорода решетки, авто-эы [) Г23 ] объясняют найденные ими ( почти на порядок меньшие, чем в случае Н2О) изменения размеров кри -: таллов Na-X при адсорбции NH3 при температуре 223 К - Предполагается, что при этой температуре первые 100 молек. III, что приводит лишь к незначительной деформации решетки. [21]
K Na) - X должны быть связаны только с атомами кислорода решетки, и поскольку энергия взаимодействия в этом случае существенно ниже, чем при адсорбции на катионах, теплота адсорбции быстро падает с заполнением. [22]
Ионы Ваа локализуются в местах пересечения каналов и координируются с 6 кислородами решетки и 4 молекулами воды. Локализация катионов в дегидратированном цеолите неизвестна, но можно предполагать, что ионы Ва2 должны сместиться в 8-членные кольца. [23]
СО-А и ВО-А-константы дисперсионного притяжения и отталкивания для взаимодействия молекулы адсорбата с атомами кислорода решетки, CS-A. Даг - л - - тоже для взаимодействия молекулы адсорбата с катионом, LIJ - расстояния между центрами молекулы адсорбата и атомов кислорода решетки, а & К-А. Поляризационная энергия Фпол определялась из расчета напряженности электрического поля, создаваемого в центре молекулы адсорбата зарядом катиона и небольшими отрицательными зарядами, которые принимались равномерно распределенными по всем атомам кислорода решетки. [24]
Повышение температуры и снижение концентрации кислорода в газовой смеси должны привести к участию кислорода решетки. [25]
Авторы работы [64] считают, что СО при образовании карбоксилатных структур реагирует с кислородом решетки. В таком случае предлагаемый ими механизм является стадийным, так как окисление СО сопровождается попеременным окислением - восстановлением поверхности. СО за счет кислорода решетки не идет. [26]
Гомомо-лекулярный изотопный обмен кислорода протекает измеримо лишь выше 450 С, обмен с кислородом решетки - выше 500 С. [27]
Изучен изотопный кислородный обмен с углекислым газом на различных контактах и показано, что кислород решетки не участвует в окис-слительном процессе при невысоких температурах. [28]
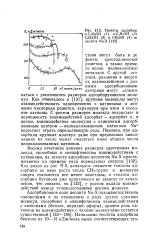 |
Теплоты адсорбцш к - С4Н9ОН ( /, н - С3Н7ОН ( 2 С2Н5ОН ( 3 и СН3ОН ( 4 ш цеолите Na-X. [29] |
Как отмечалось в [131], крупные молекулы могут взаимодействовать одновременно с катионами и атомами кислорода решетки, экранируя при этом и соседние катионы. С ростом размеров молекул возрастает и возможность взаимодействий адсорбат - адсорбат и, в целом, взаимодействие молекулы с единичным адсорбционным центром - нелокализованным катионом Na перестает играть определяющую роль. Наконец, при адсорбции крупных молекул даже при предельных заполнениях их число может оказаться ниже общего числа нелокализованных катионов. [30]
Страницы: 1 2 3 4