Кислород - решетка
Cтраница 3
В комплексообразовании СОг на поверхности катализатора участвует как кислород сорбированный на поверхности, так и кислород решетки. Но скорости кислородного изотопного обмена значительно меньше скоростей каталитических окислительных реакций. [31]
По [156], это связано с частично ковалент-ным характером связи между ионами Ag и атомами кислорода решетки. [32]
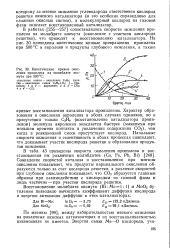 |
Кинетические кривые окисления пропилена на молибдате висмута при 500 С. [33] |
В работах i [255-257] сопоставлялись скорости окисления пропилена на модибщате висмута ( окисление с участием кислорода решетки), что приводит к восстановлению катализатора. [34]
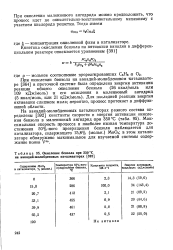 |
Окисление бензола при 350 С на ванадий-молибденовых катализаторах. [35] |
При окислении малевнового ангидрида можно предположить, что процесс идет по окислительно-восстановительному механизму с участием кислорода решетки. [36]
Наката с меченым кислородом [58] также показывают, что при высоких температурах ( 300 С) кислород решетки играет важную роль в окислении окиси углерода. [37]
Для каждого из этих окислов было показано, что окись углерода способна реагировать не только с кислородом решетки, но и с адсорбированным кислородом. Концепция необратимой хемосорбции с образованием карбонатного иона, сопровождающимся восстановлением, остается приемлемым объяснением фактов в случае взаимодействия СО с этими окислами при температурах выше 100 - 200, но при комнатной температуре можно различить другие процессы. В настоящем разделе дано описание чисто химических аспектов этой работы и показано значение полученных данных в выяснении вопроса каталитического окисления окиси углерода при низких температурах. В целом это исследование является примером классического подхода в гетерогенном катализе к фундаментальной проблеме связи каталитической активности со стабильностью адсорбированных частиц. [38]
Следовательно, реакцию можно рассматривать как два отдельно протекающих процесса: 1) удаление поверхностного кислорода или кислорода решетки ( иона), которое облегчается образованием промежуточного комплекса с окисляемой молекулой и 2) сорбцию кислорода из газовой фазы в заряженной форме. [39]
В реакции окисления метанола в формальдегид [45] избирательными могут быть катализаторы, имеющие энергетически равноценный поверхностный кислород и кислород решетки. Отмечается только, что в случае изменения состава катализатора под действием реакционной смеси возможно отклонение от данной зависимости. Другие авторы [46] отмечают, что молибдаты различных металлов, характеризующиеся относительно высокой скоростью диффузии объемного кислорода катализатора к поверхности, имеют низкую избирательность в реакции окисления пропилена в акрилонитрил. Однако эти два подхода являются своего рода следствиями из рассмотренной выше закономерности, так как опираются на энергетическое состояние кислорода катализатора. [40]
В реакции окисления метанола в формальдегид [45] избирательными могут быть катализаторы, имеющие энергетически равноценный поверхностный кислород и кислород решетки. Отмечается только, что в случае изменения состава катализатора под действием реакционной рмеси возможно отклонение от данной зависимости. Другие авторы [46] отмечают, что молибдаты различных металлов, характеризующиеся относительно высокой скоростью диффузии объемного кислорода катализатора к поверхности, имеют низкую избирательность в реакции окисления пропилена в акрилонитрил. Однако эти два подхода являются своего рода следствиями из рассмотренной выше закономерности, так как опираются на энергетическое состояние кислорода катализатора. [41]
В первом случае в промежуточном комплексе ОВК символ О означает адсорбированный кислород, а во втором случае - кислород решетки катализатора. [42]
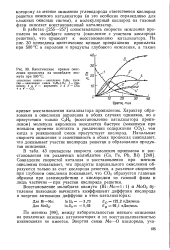 |
Кинетические кривые окисления пропилена на молибдате висмута при 500 С. [43] |
Совпадение скоростей катализа и восстановления при мягком окислении показывает, что продукты парциального окисления образуются только за счет кислорода решетки, а различие скоростей при глубоком окислении показывает, что СО2 образуется главным образом при взаимодействии с кислородом из газовой фазы и лишь частично - при участии кислорода решетки. [44]
Реакция гомомолекулярного изотопного обмена кислорода, как известно, заключается в перераспределении изотопов между двумя молекулами без участия кислорода решетки окисла. Процесс этот замечателен в том отношении, что, несмотря на большую прочность связи в молекуле кислорода ( 118 ккал / молъ), он идет с малой энергией активации при низких температурах вплоть до - 150 С. Изучение его механизма представляет поэтому принципиальный интерес для понимания причин, обеспечивающих высокую скорость низкотемпературных каталитических реакций. [45]
Страницы: 1 2 3 4