Кислород - гидроксильная группа
Cтраница 2
Далее нитрозоний-катион взаимодействует с атомом кислорода гидроксильной группы второй молекулы азотистой кислоты, который имеет неподеленные пары электронов. [16]
Образовавшийся нитрозонийкатион взаимодействует с атомом кислорода гидроксильной группы второй молекулы азотистой кислоты, который имеет неподеленные пары электронов. [17]
Сопряжение неподеленной пары электронов атома кислорода гидроксильной группы с л-электронной системой бензольного кольца приводит к смещению электронной плотности в сторону кольца. [18]
Далее нитрозошш-катион взаимодействует с атомом кислорода гидроксильной группы второй молекулы азотистой кислоты, который имеет неподеленные пары электронов. [19]
Сопряжение неподеленной пары электронов атома кислорода гидроксильной группы с я-электронной системой бензольного кольца ( р, я-сопряжение) приводит к смещению в его сторону электронной плотности. [20]
Отсюда сделан также вывод, что кислород гидроксильной группы целлюлозы не выделяется при этерифи-кации и, таким образом, остается неизменным. [21]
Это сопряжение уменьшает электронную плотность атома кислорода гидроксильной группы и тем самым увеличивает полярность - О - Н - связи, что и облегчает отщепление протона. Поэтому карбоновые кислоты проявляют значительно более сильные кислотные свойства, чем фенолы. Спирты обладают очень слабо выраженными кислотными свойствами - они практически нейтральны. [22]
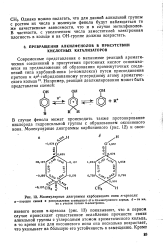 |
Молекулярные диаграммы карбониевого иона п-крезола. [23] |
В случае фенола может происходить также протонирование кислорода гидроксильной группы с образованием оксониевого иона. [24]
За первоначальным образованием полуацеталя следуют про-тонирование атома кислорода гидроксильной группы и отщепление воды с образованием оксониевого иона. Этот катион реагирует со следующей молекулой спирта, давая продукт, который превращается в ацеталь за счет потери протона. Следует отметить, что все стадии процесса обратимы и что обратная реакция также катализируется кислотой. В случае альдегидов равновесие сдвинуто в сторону образования ацеталей в отличие от аналогичной реакции кетонов, которые могут быть превращены в свои ацетали только путем удаления воды, образующейся во время реакции. Этим достигается смещение равновесия в желаемом направлении. Для этой цели обычно используется ортому-равьиный эфир ( разд. [25]
В этой реакции ] не происходит непосредственного переноса атома кислорода гидроксильной группы. Стереохимия реакции требует присоединения протона к разным концам двойной связи tyuc - аконитовой кислоты с образованием двух продуктов, поэтому тот факт, что происходит внутримолекулярный перенос трития, предполагает, что связанный tyuc - аконитат может вращаться без обмена протона с растворителем, оставаясь привязанным к ферменту. [26]
Увеличение атектронной плотности в бензольном кольце за счет влияния атома кислорода гидроксильной группы облегчает протекание реакций замещения. [27]
Ацилирование нитронафтолов ацилхлоридами в присутствии хлористого цинка происходит только по кислороду гидроксильной группы амбидентного иона. Ароматическое ядро не ацилируется. [28]
Затем происходит соединен несвободных валентностей атома углерода карбонильной группы и атома кислорода гидроксильной группы, в результате в шестичлен-ное кольцо замыкаются пять атомов углерода и один атом кислорода. В такой форме альдегидная группа отсутствует. Циклическая форма передает как порядок соединения атомов, так и их пространственное расположение. У а-формы гидроксильные группы при первом и втором углеродных атомах расположены по одну сторону кольца, у р-формы - по разные стороны кольца. Гидроксильная группа, стоящая у первого углеродного атома, наиболее реакционноспособная. [29]
Указанная поляризация происходит главным образом за счет свободных электронных пар атома кислорода гидроксильной группы ( электромерный эффект), а не за счет электронных облаков углеродных атомов алкильных групп. Следовательно, в момент реакции с наименьшей затратой энергии смещение электронов происходит, главным образом, в пара -, а не в мета-положение. В результате этого реакция в мета-положение должна протекать со значительно меньшей скоростью, чем в пара-положение, вследствие чего и невозможно образование л - нитрофе-нолов при прямом нитровании 2 4 6-триалкилфенолов. [30]
Страницы: 1 2 3 4