Карбонильный кислород
Cтраница 1
Карбонильный кислород в положении 5 триазинового кольца атакуется катионом РСЦ с образованием промежуточного оксониевого иона, который весьма неустойчив и сразу же перегруппировывается в аммонийный ион с положительным зарядом на четвертом атоме азота кольца. [1]
Карбонильный кислород в кетонах, кислотах и сложных эфирах в известной степени облегчает комплексообразование, поскольку окисленные соединения образуют комплекс при наличии менее длинной цепи, чем неокисленные. У карбоновых кислот способность образовывать комплексы проявляется, начиная с масляной кислоты, у кетонов - с ацетона, у спиртов - с гексанола. [2]
Карбонильный кислород в кетонах, кислотах и сложных эфирах не только не препятствует образованию комплексов, но, по-видимому, облегчает комплексообразование, так как окисленные соединения с более короткими углеродными цепями дают комплексы. Ацетон с тремя углеродными атомами в прямой цепи, масляная кислота с четырьмя углеродными атомами и их высшие гомологи образуют комплексы с мочевиной. [3]
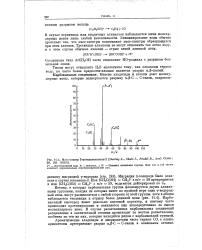 |
Масс-спектр З - метилпентанона-2 Sharkey А Shulz /., Friedel Д., Anal. Chem., 28, 931 ( 1956 ]. [4] |
Карбонильный кислород имеет довольно основной характер, и поэтому часто происходит протонирование и появляется пик непосредственно за пиком молекулярного иона. В случае разветвленных карбонильных соединений расщепление в значительной степени происходит по местам разветвления, особенно по тем из них, которые находятся рядом с карбонильной группой. [5]
Каждый карбонильный кислород и амидный азот включены в водородную связь. [6]
При замене карбонильного кислорода на серу снижается фито-токсичность соединений, тогда как при замене его на иминогруппу образуются активные гербициды - производные изомочевины. [7]
Обычное протонирование карбонильного кислорода приводит к увеличению положительного заряда на углероде, что способствует нукле-офильной атаке воды по этому положительно заряженному центру. [8]
Образующаяся из карбонильного кислорода гидроксильная группа на ы-иаотся карбонильным ( или глюкозидным) гидроксилом. Он отличается от других гидроксильных групп большей способностью к реакциям. [9]
Реакции замещения карбонильного кислорода у моноз протекают при действии фенилгидразина, а также гидроксиламина. Особенное значение имеет реакция с фенилгидразином, которая применяется для разделения моноз. Реакция протекает в 3 стадии: 1) сначала образуются гидразоны при действии одной молекулы фенилгидразина; 2) при действии второй молекулы фенилгидразина окисляется соседняя с карбонильной группой спиртовая группа с образованием карбонильной группы; 3) последняя реагирует с третьей молекулой фенилгидразина с образованием нерастворимого фенил-озазона. [10]
Обмен между карбонильным кислородом и водой оказывается значительным, поскольку возврат тетраэдри-ческого интермедиа та к исходным реагентам протекает быстрее, чем разложение с образованием продуктов. [11]
В результате окисления карбонильный кислород появляется у того же атома углерода, у которого раньше находилась нитрогруппа. [12]
Обмен азота на карбонильный кислород имеет очень небольшое препаративное значение. Используемые при этом методы не всегда применимы. [13]
Неподеленные пары электронов карбонильного кислорода придают карбонильной группе свойства слабого основания Льюиса. [14]
Большинство реакций замещений карбонильного кислорода, обычно сопровождаемых отщеплением воды, также протекает через стадию присоединения. [15]
Страницы: 1 2 3 4