Исследованная кислота
Cтраница 1
Исследованные кислоты располагают в ряд по возрастающей степени кислотности. Различие в концентрации растворов может несколько отразиться на положении отдельных кислот в полученном ряду. [1]
Исследованные кислоты сильно различаются по степени диссоциации; в гл. V рассмотрены причины такого различия. Для всех кислот спектроскопические данные позволяют воссоздать гидратные структуры в зависимости от степени гидратации. Особый интерес представляют результаты, относящиеся к гидратации избыточного диссоциированного протона. Группы Н5Ог и HgOJ занимают особое положение среди гидратных структур. [2]
Располагают исследованные кислоты в ряд по возрастающей степени кислотности. Различие в концентрации ( нормальности) растворов может несколько отразиться на положении отдельных кислот в полученном ряду. [3]
Адсорбция всех исследованных кислот ноеит обратимый характер. [5]
Проведено сравнение комплексообразующих свойств исследованной кислоты со свойствами этилендиаминдиметил-карбоновой и этилендиаминдиизопропилфосфоновой кислот. [6]
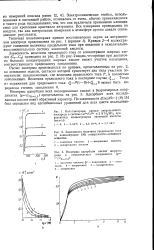
Так как для двух других исследованных кислот в изученных интервалах температуры с повышением ее величина PD / - Рн растет, то можно предположить, что при более высоких температурах и для этих веществ будет наблюдаться максимум отношения давлений пара. Так как этот эффект по знаку противоположен изотопному эффекту для D20, ND3 и CH3OD, но, наоборот, одинаков с таковым дляСН3СОСШ, то данные [312], возможно, означают, что около. С азотная кислота в значительной степени ассоциирована и в газовой. [7]
По составу образующихся комплексов все исследованные кислоты распадаются на три группы. [8]
Данные таблицы показывают, что исследованные кислоты при 70 - 80 С и давлении до 300 am в метане не растворяются. При повышении давления до 400 - 500 am наблюдается их слабое растворение. [9]
По скорости отщепления карбоксильной группы исследованные кислоты располагаются в такой ряд [120]: уксуснаявалериановая муравьиная бензойная. [10]
Из табл. 26 следует, что исследованные кислоты при 70 - 80 С и давлениях до 300 кгс / см2 в метане не растворяются. При повышении давления до 400 - 500 кгс / см2 наблюдается их слабое растворение. [11]
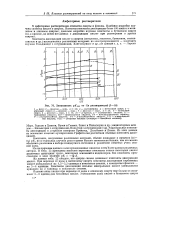 |
Зависимость рДГ0тн от 1 / 8 растворителей ( 1 - 10. [12] |
Мы не приводим данных о всех исследованных кислотах и тем более данных различных авторов. В табл. 22 приведены наиболее вероятные константы только некоторых кислот различных природных групп, некоторых оснований и индикаторов. Все константы представлены в виде величин рК - lg К. [13]
Мы не приводим данных о всех исследованных кислотах и тем более данных различных авторов. В таблице 63 приведены наиболее вероятные константы только некоторых кислот, различных природных групп, некоторых оснований и индикаторов. [14]
Мы не приводим данных о всех исследованных кислотах и тем более данных различных авторов. В табл. 24 приведены наиболее вероятные константы только некоторых кислот различных природных групп, некоторых оснований и индикаторов. [15]
Страницы: 1 2 3