Исследованная кислота
Cтраница 2
В табл. 23 приведены свойства двух наиболее хорошо исследованных кислот - трифторуксусной и гептафтор-масляной, в сравнении со свойствами соответствующих незамещенных кислот. [16]
По-видимому, такой эффект связан с полирующим действием исследованных кислот по отношению к поверхности металла ( что и наблюдалось у пластинок в этих опытах) при одновременном разрушающем действии этих кислот на антикоррозионную присадку. Последнее подтверждается ходом кривых справа от минимумов, когда, несмотря на увеличение количества пленки и времени ее существования на поверхности свинца, резко увеличивается его коррозия. Это, по-видимому, связано с имеющим место при разрушении присадки переходом серы в более реакционно способное состояние, в котором она не обладает антикоррозионными свойствами, а взаимодействуя с поверхностью свинца, вызывает интенсивное коррозионное разрушение последней. [17]
Одновременно получение кислоты С8Н1ЬСООН указывает на отсутствие в исследованных кислотах таких кислот, у которых карбоксильная группа непосредственно связана с циклической частью молекулы. [18]
Отсюда следует, что зависимость ассоциации от степени гидратации в ряду исследованных кислот характеристична. Она увеличивается на порядок при переходе от полистиролсульфо-новой к полистиролфосфиновой кислоте. [19]
Приведенные в табл. 29 результаты выбраны для того, чтобы показать разнообразие исследованных кислот и использованных методов. [20]
Таким образом, предположение о постоянстве концентрации катализатора в ходе полимеризации неверно ( по крайней мере для исследованных кислот) и понижение скорости на ранних стадиях реакции вызвано не образованием сильно основного дим ер а, а объясняется снижением концентрации катализатора. Расход катализатора при полимеризации с НС1, НВг, H2SO4, анионы которых могут конкурировать с молекулой имина в раскрытии протонизированного этилениминного кольца, - не является неожиданным, поскольку каждая из этих кислот способна реагировать с этиленимином, образуя продукты раскрытия цикла. [21]
Полосы мономеров детально исследовались при этих условиях Гулденом [54], который указывает для них интервал от частоты 3504 см 1, соответствующей полосе фторуксусной кислоты, наиболее сильной из исследованных кислот, до 3545 см 1, соответствующей полосе наиболее слабой п - yV - диметиламинобензойной кислоты. Эта зависимость частоты от силы кислоты отражает роль индукционных эффектов заместителей при карбоксильной группе, которые влияют как на частоту, так и на величину рК.а. Значения частот колебаний ОН и величин рКа связаны для отдельных рядов алифатических, ароматических и р у-непредельных кислот простой линейной зависимостью. Были также приближенно измерены коэффициенты погашения некоторых полос мономеров, причем было найдено, что величина их составляет примерно лишь одну пятую от соответствующего значения для фенолов. [22]
Виноградовым [1554] отмечено повышение скорости полимеризации стирола под влиянием диазоаминобензола, при добавлении органических кислот или их ангидридов, ускоряющих процесс распада диаминобензола. Исследованные кислоты по активности в процессе полимеризации, располагаются в следующий ряд: монохлоруксусная муравьиная уксусная бензойная, масляная олеиновая. [23]
Среди уже исследованных кислот следует отметить трифторуксусную СРз СООН и борфторуксусную ВР3 ( СН3СООН) кислоты. Соли таких кислот были получены как с заполнением всех слоев, так и с меньшим числом внедренных атомов. [24]
Появление окраски в ацетоновом растворе позволяет и в этих системах предположить перенос заряда не по механизму Н - связи. Наименее активной из исследованных кислот оказалась фталевая, так как в данном случае при гетерогенном взаимодействии не было обнаружено привеса. [25]
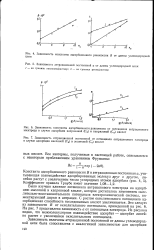
Было изучено влияние потенциала антраценового электрода на адсорбцию масляной и капроновой кислот, которое достигалось изменением окислительно-восстановительного потенциала электрохимической системы, инжектирующей дырки в антрацен. С ростом окислительного потенциала адсорбционная способность исследованных кислот увеличивается. На рис. 7 представлена зависимость а от потенциала электрода. Из рисунка видно, что межмолекулярное взаимодействие адсорбат - адсорбат линейно растет с увеличением окислительного потенциала. [27]
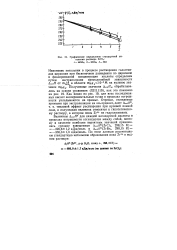 |
Графическое определение стандартной энтальпии раствора ZrCU. / - НСЮ. 3 - HNO. 3 - НС1. [28] |
Изменение энтальпии в процессе растворения галогени-дов циркония при бесконечном разведении по цирконию и фиксированной концентрации кислоты определяем путем экстраполяции прямолинейной зависимости hsotH от т в области mzrx410 - 3M на нулевое значение mzrx4 - Полученные значения Д Я обрабатывались на основе уравнения ( XIII. Как видно из рис. 19, для всех исследованных кислот экспериментальные точки в пределах погрешности укладываются на прямые. [29]
Таким образом, с учетом ранее представленных данных по гидролизу сложных вго / 7-бутиловых эфиров карбоновых кислот, можно сделать вывод о том, что, с точки зрения процесса получения бутанола-2 из н-бутенов, наиболее выгодно применять уксусную кислоту. Ее преимущества обусловлены и тем, что она единственная из исследованных кислот не дает азеотропа с водой [8], что имеет большое значение для разделения продуктов реакции. [30]
Страницы: 1 2 3