Разбавленная хлорная кислота
Cтраница 1
Разбавленная хлорная кислота не проявляет окислительных свойств ни на холоду, ни при нагревании. Горячая концентрированная хлорная кислота ( 60 - 72 % - ная) является сильным окислителем. [1]
Разбавленная хлорная кислота слабо действует на уран, но при концентрировании ее, например при удапении воды кипячением, можно добиться бурной реакции. [2]
Разбавленная хлорная кислота практически не проявляет окислительных свойств. Иногда к концу разложения начинают выделяться оранжево-красные кристаллики хромовой кислоты, которые, обволакивая неразложившиеся еще частицы пробы, затрудняют дальнейшее их разложение. В этом случае рекомендуется охладить раствор, прилить 2 - - 3 мл воды и снова нагреть до появления паров хлорной кислоты. [3]
Разбавленная хлорная кислота практически не проявляет окислительных свойств. Иногда к концу разложения начинают выделяться оранжево-красные кристаллики хромовой кислоты, которые, обволакивая неразложившиеся еще частицы пробы, затрудняют дальнейшее нх разложение. В этом случае рекомендуется охладить раствор, прилить к нему 2 - 3 мл воды и снова нагреть до появления паров хлорной кислоты. [4]
Разбавленная хлорная кислота практически не является окислителем; ее окисляющее действие проявляется только в достаточно концентрированных растворах и при нагревании. [5]
Если разбавленную хлорную кислоту нагревать в отсутствие восстановителей, она постепенно концентрируется, превращаясь в азеотропную смесь ( дигидрат), содержащую 72 % кислоты и кипящую при 203 С. Следовательно, безводная хлорная кислота, которая отличается значительной неустойчивостью и при хранении самопроизвольно взрывается ( ее можно хранить только при очень низких температурах), не может быть получена простым кипячением. Однако горячая концентрированная хлорная кислота тоже может давать сильные взрывы в присутствии определенного типа органических веществ, а именно - этилового спирта, целлюлозы, полиспиртов. Причина этого - образование этилперхлората, обусловленное дегидратирующим действием горячей концентрированной кислоты. Поэтому к холодному раствору хлорной кислоты сначала добавляют азотную кислоту, а затем постепенно нагревают. Большая часть органических веществ разрушается азотной кислотой, которая в конечном счете испаряется из смеси. [6]
Если разбавленную хлорную кислоту нагревать в отсутствие восстановителей, она постепенно концентрируется, превращаясь в азеотрштную смесь, содержащую 72 5 % кислоты. Следовательно, безводная хлорная кислота, которая отличается значительной неустойчивостью и при хранении самопроизвольно взрывается ( ее можно хранить только при очень низких температурах), не может быть получена простым кипячением. Однако горячая концентрированная хлорная кислота тоже может давать сильные взрывы в присутствии определенного типа органических веществ, а именно - этилового спирта, целлюлозы, полиспиртов. Смит считает причиной этого образование этилперхло-рата, обусловленное дегидратирующим действием горячей концентрированной кислоты. [7]
Устойчивую соль H3UrNaH2UrH2O можно легко перекристаллизовать из разбавленной хлорной кислоты и применять для удаления иона натрия из раствора. Анион урамилдиуксусной кислоты ведет себя, вероятно, как три - или тетрадентатный ли-ганд, предпочтительно образуя комплексы тетраэдрического строения. Это может объяснить, почему комплексы с Li, Na и Be ( log / ( ML 10 36) прочнее комплексов EDTA, в то время как комплексы с большинством двухзарядных катионов слабее. В соответствии с этим предположением находится и то наблюдение, что образование NTA более прочных комплексов, чем имино-диуксусной кислотой, объясняется главным образом превращением тридентатного хелатообразующего реагента в тетрадентатный. Введение в положения 1 и 3 HsUr метальных групп оказывает очень слабое влияние на константы устойчивости комплексов Li, Na, К и Т1, что позволяет предположить [47] образование лигандом стерически предпочтительной конфигурации со структурой типа клетки, допускающей размещение малых ионов и делающей более предпочтительным тетраэдрическое их окружение. [8]
Растворяют 25 г чистого карбоната кальция в разбавленной хлорной кислоте, избегая избытка, и разбавляют до 500 мл водой. [9]
Чистый субстрат не изменяется при кипячении в разбавленной хлорной кислоте, однако небольшие концентрации галоге-нид-ионов приводят к быстрому протолизу даже при 0 С. В приводимой интерпретации предполагается, что за предравновесным захватом двух хлорид-ионов следует предравновесие протолиза ртутного остатка. Органический продукт автоматически перегруппировывается, в результате чего образуется енольная форма карбэтоксигрушш. Возврат в обычную форму, вероятно, происходит не быстро ( гл. XI) и катализируется ионами водорода. Это объясняет, почему в выражение для скорости входит концентрация ионов водорода во второй степени. [10]
Хорошо растворимые перхлораты готовят, растворяя в разбавленной хлорной кислоте металлы, их гидроксиды или карбонаты. [11]
Для разложения карбонатов и некоторых сульфидов широко используется разбавленная хлорная кислота. [12]
Возможное объяснение различия в изотопных эффектах для серной кислоты и разбавленной хлорной кислоты состоит в том, что в хлорной кислоте реагентом является только ион гидроксония, а в серной кислоте ( 6 3 М) это H2S04 и HSOJ, причем известно, что более слабой кислоте соответствует больший изотопный эффект. [13]
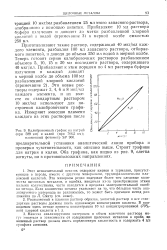 |
Калибровочный график на натрий. [14] |
Прибавляют 10 мл раствора буфера излучения и доводят до метки разбавленной хлорной кислотой и водой ( примечание 3) в мерной колбе емкостью 250 мл. [15]
Страницы: 1 2 3