Льюисовская кислота
Cтраница 1
Льюисовская кислота представляет собой акцептор пары электронов, в отличие от кислоты по Бренстеду - донора протона. Основание по Бренстеду является акцептором протона. [1]
Льюисовские кислоты SnCl4, TiCl4 не являются электролитами, хотя их растворы в ацетилхлориде лучше проводят электрический ток, чем сам растворитель. [2]
Льюисовские кислоты не вызывают полимеризации в отсутствие сокатализатора. Способность лактонов полимеризации уменьшается в ряду: б-валеролактон е-капролактон р-пропиолактон. Из данных по содержанию СООН-групп в по лимере сделан вывод о том, что полимеризация идет через ациль-ное, а не алкильное раскрытие лактонного кольца. [3]
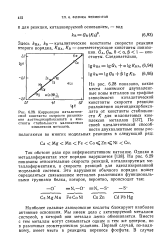 |
Корреляция каталитической константы скорости разложения ацетондикарбоксилата и константы стабильности малонатовых комплексов металлов. [4] |
Наиболее сильные льюисовские кислоты блокируют наиболее активные основания. Мы имеем дело с активируемой металлом системой, в которой ион металла легко обменивается. Вместе с тем металлы могут связываться одним и тем же центром, но в различных геометрических условиях. Первый случай, по-видимому, имеет место в реакциях переноса фосфата. [5]
Льюисовских кислот ( SO3, SnCl4, SbCl3, SbCl5 и др.) и энтальпии нейтрализации их а-гшколином, диметилани-лином, хинолином и пиридином, также не представляют для нас большого интереса. [6]
 |
Координационные числа некоторых ионов металлов. [7] |
Среди льюисовских кислот наибольший интерес для биологов представляют ионы металлов. Однако координационную связь могут образовывать не только поливалентные ионы. Ионы щелочных металлов также обнаруживают определенную тенденцию к образованию координационных соединений, что во многом объясняет влияние ионов К и Na на активность ряда ферментов. Известны и нечетные координационные числа ( 3, 5, 7), однако они встречаются реже. [8]
Так как льюисовские кислоты присоединяются к молекулам оснований по месту наибольшей электронной плотности последних, то их называют электрофильными реагентами. Аналогично, льюисовские основания, всегда атакующие другие молекулы в том месте, где атомные ядра наименее экранированы электронами, называются нуклеофильны-ми реагентами. [9]
Продукты присоединения льюисовских кислот к ангидридам и хлоран-гидридам ( как к основаниям) известны уже давно [277], и нет сомнения в том, что катализ в реакции Фриделя - Крафтса связан с образованием такого рода соединений. [10]
Нитробензол является слабой льюисовской кислотой, так как способен образовывать л-комплексы, например с ароматическими аминами [585, 595] Смесь нитробензола с анилином приобретает желтую окраску из-за образования комплекса с переносом заряда. [11]
Только триметилалюми-ний - очень сильная Льюисовская кислота - связывается с три-силиламином. [12]
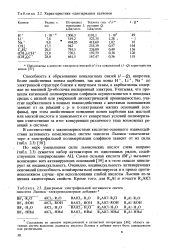 |
Характеристики однозарядных катионов.| Диаграмма электрофильной активности систеи кислота Льюиса-электронодонорная добавка. [13] |
По мере уменьшения силы льюисовских кислот слева направо ( табл. 2.3) сужается набор активаторов из однотипных рядов, содействующих генерированию АЦ. Самая сильная кислота ( BF3) вызывает ионизацию всех активирующих оснований [59] и в этом смысле нивелирует их индивидуальность. Очевидно, индивидуальность активирующих оснований ( способность ионизироваться) нивелируется и в прямо противоположном случае-при использовании слабой кислоты Льюиса из-за низких акцепторных свойств. [14]
По мере уменьшения силы льюисовских кислот слева направо сужается набор активаторов из однотипных рядов, содействующих генерированию активных центров. Самая сильная кислота BF3 вызывает ионизацию всех активирующих оснований [26, 27] и в этом смысле нивелирует их индивидуальность. [15]
Страницы: 1 2 3 4