Лимонная кислота
Cтраница 1
Лимонная кислота применяется при крашении и ситцепечатании, в медицине в виде соли ( цитрат железа), а главным образом при приготовлении напитков и кондитерских изделий для придания им приятного кислого вкуса. [1]
Лимонная кислота применяется при крашении и ситцепечатании, в медицине в виде соли ( цитрат железа), а главным образом при приготовлении напитков и кондитерских изделий для приданий им приятного кислого вкуса. [2]
Лимонная кислота не содержит групп атомов (15.3) и (15.7), поэтому она но способна подвергаться непосредственному дегидрированию. Пройдя две стадии предварительной активации, она преобразуется в изолимонную кислоту, содержащую группу атомов (15.3), которая и подвергается дегидрированию. В последующих процессах дегидрирования, декарбоксилирования и активации молекул с помощью кофермента А выделяются две молекулы С02 и 8 атомов водорода. В настоящее время установлено, что конечным этапом метаболизма жирных кислот, аминокислот и углеводов является цикл Кребса. [3]
Лимонная кислота по силе действия на фосфорнокаль циевую соль приближается к той кислоте, которая выделяется корнями растений при соприкосновении их с минеральными веществами почвы. [4]
Лимонная кислота составляет более половины всех потребляемых в пищевой промышленности органических кислот. В начале 80 - х годов суммарные мощности по ее производству более чем в 30 капиталистических странах, по оценке, превышали 500 тыс. т / год, а ежегодное производство колебалось в пределах 370 - 400 тыс. т, при этом более / з вырабатывалось в США. [5]
Лимонная кислота ( ГОСТ 908 - 41) - бесцветные или слегка желтоватые кристаллы 2-окси - 1, 2, 3-пропантрикарбоновая кислота, температура кипения - 153 С. Получается при лимоннокислом брожении сахара или экстрагированием из плодов растений и махорки. [6]
Лимонная кислота применяется в кондитерском деле, в фотографии и для консервирования крови. [7]
Лимонная кислота широко применяется в пищевой промышленности, а также при крашении, в медицине и других областях. [8]
Лимонная кислота растворима в воде и этиловом спирте, поэтому ее можно применять в смеси с ним для выведения пятен. Чаще всего лимонную кислоту используют для удаления пятен с шелковых тканей. [9]
Лимонная кислота при нагревании с концентрированной серной кислотой дает ацстондикарбоновую кислот и поэтому некоторые исследователи предпочитают применять для конденсации с фенолами лимонную кислоту вместо чистой ацетон-дикарбоновой кислоты. Ti о - и n - аминофенолы - совсем ire вступают в реакцию. Таким Образом, замещенные ацегоуксусные эфиры, содержащие карбо-ксилыгую и карбэток-сильную группы в у-положении, более активны, чем у-этил - или у-фенилзамещенные. [10]
Лимонная кислота в этих условиях практически не поглощается. [11]
Лимонная кислота применяется при крашении тканей, в кондитерском производстве. В медицине лимонная кислота используется для приготовления кровяной плазмы при переливании крови ( цитратная плазма), в качестве противоядия при отравлении щелочами, а также в виде соли железа - как препарат, назначаемый при малокровии. [12]
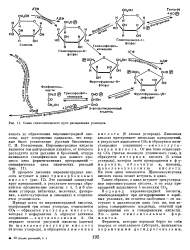 |
Схема гликолитического пути расщепления углеводов. [13] |
Лимонная кислота претерпевает несколько превращений, в результате выделяется ССЬ и образуется пяти-углеродное соединение - а-к етоглута-ровая кислота. От нее тоже отщепляется СО2 ( третья молекула углекислого газа), и образуется янтарная кислота ( 4 атома углерода), которая затем превращается в ф у-маровую, яблочную и, наконец, щавелевоуксусную кислоту. На этом цикл замыкается. Щавелевоуксусная кислота снова может вступить в цикл. [14]
Лимонная кислота в пересчете на СвНеОт Н2О 99; зола 0 5; свободная серная кислота 0 05; мышьяк 0 00014; не должна содержать алкалоиды и ионы тяжелых металлов, железистосинеродисто-водородной кислоты, бария и щавелевой кислоты. [15]
Страницы: 1 2 3 4