Марганцоватистая кислота
Cтраница 1
Марганцоватистые кислоты в свободном виде не выделены, а соответствующие им соли манганиты ( Na2MnO3, Ca2MnO4 и др.) образуются при сплавлении двуокиси марганца с основными оксидами. [1]
Осаждеяная марганцоватистая кислота растворяется в растворе кислого щавелевокислого алия, давая великолепное красное окрашивание раствора, обусловленное образованием комплексного иона марганца и щавелевой кислоты. [2]
Осажденная марганцоватистая кислота растворяется в растворе кислого щавелевокислого алия, давая великолепное красное окрашивание раствора, обусловленное образованием комплексного иона марганца и щавелевой кислоты. [3]
Соли марганцоватистой кислоты Н2МпО3 называются манганитами. [4]
От марганцоватистой кислоты [ и Мп ( ОН) 2 как основания ] производится встречающийся в природе темно-красный минерал гаусманит: 2Мп ( ОН) 24 - Н4МпО4 МлгМг. Таким образом, с химической точки зрения гаусманит ( Мп3О4) является манганатом марганца. [5]
Фильтр с осадком марганцоватистой кислоты для ускорения растворения последней размешивают стеклянной палочкой при нагревании. Отсутствие коричневого осадка в стакане и на фильтре указывает на конец реакции. Избыток щавелевой кислоты оттитровывают раствором марганцовокислого калия. На основании приведенной реакции мы видим. [6]
При стоянии на воздухе Мп медленно окисляется, превращаясь в нерастворимую бурую марганцоватистую кислоту НгМпОз, которая выпадает в осадок; если раствор остается на воздухе достаточно долго, то весь Мп выделится в осадок. Такое поведение Мп следует учесть при отделении его от трехвалентных металлов А1, Сг и Fe. NFhCl; раствор следует прокипятить для полного удаления растворенного воздуха, добавить лишь небольшой избыток NHs и выпавший осадок центрифугировать возможно быстрее. [7]
Если полученный зеленый раствор нагреть, он буреет и выделяет бурый осадок марганцоватистой кислоты МпО ( ОН) 2 ( см. стр. [8]
При окислении в щелочной или нейтральной среде семивалентный марганец восстанавливается до четырехвалентного, причем образуется марганцоватистая кислота Н3МпО3, выпадающая в виде бурого осадка. [9]
Когда в пробе появляются нитриты ( в последний период инкубации), тотчас же после растворения осадка марганцоватистой кислоты в колбу для титрования прибавляют 1 г бикарбоната натрия и оттитровывают выделившийся иод тиосульфатом натрия. [10]
Когда в пробе появляются нитриты ( в последний период инкубации), тотчас же после растворения осадка марганцоватистой кислоты в колбу для титрования прибавляют 1 г бикарбоната натрия и оттитровывают выделившийся иод тиосульфатом натрия. [11]
Последнее уравнение показывает образование МпМпОз при действии неизменившейся и имеющей основной характер Мп ( ОН) а на марганцоватистую кислоту, получающуюся по второму из указанных уравнений. [12]
Как показывает последнее уравнение, часть образовавшегося за счет окисления Мп ( ОН) 2 гидрата двуокиси марганца ( марганцоватистой кислоты), взаимодействуя с неокисленным гидратом основного характера, дает соль, называемую манганитом. [13]
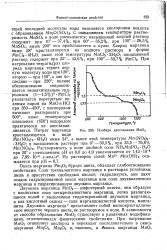 |
Изобара диссоциации МпО2. [14] |
Двуокись марганца МпО2 - амфотерный окисел; она образует с кислотами соли четырехвалентного марганца, легко разлагающиеся водой с выделением гидратированной двуокиси марганца, а как кислотный окисел - соли марганцоватистой кислоты, манга-йиты. Двуокись марганца7 представляет собой мелкокристаллическое вещество черного цвета, не растворимое в воде. В зависимости от способа образования МпО2 существует в различных модификациях, отличающихся физическими свойствами. [15]
Страницы: 1 2 3