Марганцоватистая кислота
Cтраница 2
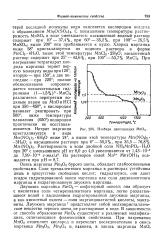 |
Изобара диссоциации МпОа. [16] |
Двуокись марганца Мп02 - амфотерный окисел; она образует с кислотами соли четырехвалентного марганца, легко разлагающиеся водой с выделением гидратированной двуокиси марганца, а как кислотный окисел - соли марганцоватистой кислоты, манга-ниты. Двуокись марганца 7 представляет собой мелкокристаллическое вещество черного цвета, не растворимое в воде. В зависимости от способа образования Мп02 существует в различных модификациях, отличающихся физическими свойствами. [17]
Двуокись марганца Мп О2 - амфотерный окисел; она образует с кислотами соли четырехвалентного марганца, легко разлагающиеся водой с выделением гидратированной двуокиси марганца, а как кислотный окисел - соли марганцоватистой кислоты, манганиты. Двуокись марганца3 представляет собой мелкокристаллическое вещество черного цвета, нерастворимое в воде. В зависимости от способа образования МпО2 существует в различных модификациях, отличающихся физическими свойствами. [18]
Наиболее устойчивыми в водном растворе являются розоватый Мп2, многие соли которого хорошо растворимы в воде ( например, MnSO4, Mn ( NO3b, МпС12 и др.), черная нерастворимая в воде марганцоватистая кислота Н2МпО3, или МпО ( ОН) 2 ( ее ангидрид МпО2 - двуокись марганца), и фиолетовый перманганатный ион МпОГ, все соли которого хорошо растворимы в воде. Изучаемый нами ион Мп2 обнаруживается главным образом с помощью окислительно-восстановительных реакций, например окислением его до МпОГ, обладающего характерной окраской и резко выраженными окислительными свойствами. [19]
По охлаждении раствора к нему приливают 200 мл воды, нагревают до кипения, затем приливают 25 мл 20 % - ного раствора надсернокислого аммония и продолжают кипятить в течение 15 - 20 минут, при этом весь марганец окисляется в марганцоватистую кислоту и выпадает в виде осадка. Избыток надсернокислого аммония разрушают кипячением раствора в течение 10 - 15 минут. Прекращение выделения пузырьков газа служит признаком конца разложения. Выделившийся осадок двуокиси марганца переносят на фильтр и промывают 4 - 5 раз горячей водой. [20]
Под влиянием марганцовати-стой кислоты из n - толуидина образуется окрашенный продукт окисления. Сама марганцоватистая кислота получается окислением Мп ( ОН) 2 кислородом воздуха. [21]
В кислотах растворяется с образованием солей четырехвалентного марганца, легко разлагаемых водой с выделением гидра-тированной двуокиси Мп. Со щелочами образует соли марганцоватистой кислоты - манганиты. [22]
На течение реакции оказывает большое влияние кислотность среды. При недостаточной кислотности образуется темно-бурый осадок марганцоватистой кислоты. [23]
Ее соли-манганиты-легко гидролизуются водой с выделением бурого осадка марганцоватистой кислоты. [24]
Ее соли-гманганиты легко гидролизуются водой с выделением бурого осадка марганцоватистой кислоты. [25]
Ее соли-манганиты легко гидролизуются водой с выделением бурого осадка марганцоватистой кислоты. [26]
Ее соли - манганиты легко гидролизуются водой с выделением бурого осадка марганцоватистой кислоты. [27]
Ее соли - манганиты легко гидролизуются водой с выделением бурого осадка марганцоватистой кислоты. Сильные окислители в щелочной среде ( в растворах или при сплавлении) переводят соединения Мп4 в соли шестивалентного марганца - щ манганаты. [28]
Ее соли - манганита - легко гидроли-зуются водой с выделением бурого осадка марганцоватистой кислоты. [29]
Гидрат окиси марганца ( 1У) имеет большую реакционную способность, чем безводная форма. С сильными основаниями он образует лш гаяаты ( 1У) ( соли гипотетической марганцоватистой кислоты), а с кислотами дает соли Mn ( IV), поэтому считают, что он имеет амфотерный характер. Эти соединения по аналогии с другими веществами, получаемыми сухим путем, следует рассматривать скорее как смешанные окиси. Продукты реакции гидрата окиси марганца ( 1У) со щелочами в водных растворах не имеют определенного стехиометрического состава, и возможно, что они представляют собой продукты адсорбции щелочи коллоидным гелем. [30]
Страницы: 1 2 3