Оксикоричная кислота
Cтраница 3
В цветках растений, бутоны которых развивались в темноте, не найдено заметных количеств антоциана, однако они содержали в высокой концентрации п-оксифенилпировиноградную кислоту. Шмидт предположил, что свет блокирует превращение и-оксифенил-пировиноградной кислоты в n - оксикоричную кислоту. По другим данным п-оксифенилпировиноградная кислота не является промежуточным продуктом при синтезе флавоноидов. [31]
Оксикоричные кислоты встречаются в природе в большем числе сложных соединений, нежели любая другая группа растительных фенолов. Обычные коричные кислоты ( - кумаровая, феруловая, кофейная и синаповая) могут быть связаны с сахарами гликозидными связями, сложноэфирными связями или и теми, и другими. Кроме Сахаров, найдено значительное число других органических молекул, присоединяющихся к оксикоричным кислотам; к ним относятся циклогексанокарбоновые кислоты, например хинная, органические кислоты, например винная, С6 - С3 - соединения, флавонолы, антоцианидины, С-гликозиды флавонов, терпеноиды и алкалоиды. В следующих пяти параграфах будут рассмотрены эти различные комбинированные формы. [32]
Однако в случае, когда 7-океигруппа замещена, под влиянием щелочей флава-й Ойы легко изомеризуются до халкойов, что видно по батогромно-му сдвигу максимума первой полосы на 100 - - 120 ммк [ 4, 75; Слв-дувт отметить, что раньше в обзорах Аршова [76] и Скаржинского 177 ] указывалось на то, что ацшгарование 4 -оксигруппы приводит к гипсохромии максимума длинноволновой полосы. Это замечание справедливо с тем исключением, что не все ацильные заместители приводят к такому явлению. Например, в последнее время были обнаружены апигениновые соединения, ацилированные в 4 -поло-жении оксикоричными кислотами [18, 19], у которых не наблюдается гипсохромии. [33]
Оказалось, что полимер из феруловой кислоты очень сильно напоминает натуральный лигнин, и это еще более подтвердило гипотезу о том, что in vivo это соединение является хорошим предшественником лигнина. Стаффорд предположил, что отличие результатов, полученных с коричной кислотой и тирозином, от результатов Брауна и Ней-ша [30] может быть следствием или медленного превращения этих соединений в n - оксикоричную кислоту, или ингибирования перекисью ферментативных реакций, или использования субстратов в конкурентных реакциях. [34]
В обзоре Нейша [3] рассмотрена роль коричной кислоты и ее оксипроизвод-ных в биосинтезе многих фенолов. Нейш обсудил возможную роль фенилмолоч-ной кислоты в образовании коричной кислоты. Предложена последовательность реакций, включающая переаминирование фенилаланина, восстановление кетокислоты до фенилмолочной кислоты и дегидратацию последней с образованием коричной кислоты. По аналогии была предложена последовательность для превращения тирозина в n - оксикоричную кислоту, причем дегидратация n - оксифенилмолочной кислоты является конечной стадией у злаковых. [35]
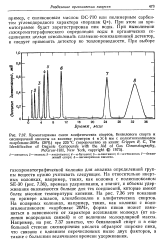
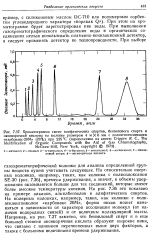
На относительно инертных колонках, например, таких, как колонка с полисилоксаном SE-30 ( рис. 7.36), времена удерживания, а значит, и объемы удерживания оказываются больше для тех соединений, которые имеют более высокие температуры кипения. На рис. 7.36 это показано на примере алканов, алкилбензолов и алифатических спиртов. На полярных колонках, например, таких, как колонки с полиэтиленгликолем карбовакс 20М, форма пиков может изменяться в зависимости от характера ассоциации молекул ( от наличия водородных связей) и от величины молекулярной массы. Например, на рис. 7.37 заметно, что бензиловый спирт и в еще большей степени оксикоричная кислота образуют широкие пики, что связано с влиянием перечисленных выше двух факторов, а также с большими величинами времени удерживания. [37]
На относительно инертных колонках, например, таких, как колонка с полисшюксаном SE-30 ( рис. 7.36), времена удерживания, а значит, и объемы удерживания оказываются больше для тех соединений, которые имеют более высокие температуры кипения. На рис. 7.36 это показано на примере алканов, алкилбензолов и алифатических спиртов. На полярных колонках, например, таких, как колонки с полиэтиленгликолем карбовакс 20М, форма пиков может изменяться в зависимости от характера ассоциации молекул ( от наличия водородных связей) и от величины молекулярной массы. Например, на рис. 7.37 заметно, что бензиловый спирт и в еще большей степени оксикоричная кислота образуют широкие пики, что связано с влиянием перечисленных выше двух факторов, а также с большими величинами времени удерживания. [39]
Можно не принимать во внимание более ранние сообщения о наличии свободных фенолов в тканях листьев и цветков, так как в то время не принималось достаточных мер предосторожности для исключения ферментативного или кислотного гидролиза гликозидов при выделении. Единственная группа фенольных соединений, которые не связываются с сахарами с образованием гликозидов - это полимерные лигнины и лейкоантоцианидины. Однако лигнин встречается в стенках клетки в тесной связи с полисахаридом - целлюлозой; такая же комбинация возможна и в случае лейкоантоцианидинов. В низших растениях, и особенно у бактерий и грибов, фенольные соединения ( например, антрахиноны, оксикоричные кислоты и фенолокислоты) обычно не присоединены к сахарам. Немногие фенольные соединения, обнаруженные в животном мире, обычно также находятся в свободном состоянии, хотя из некоторых насекомых были выделены гликозиды. [40]
Для этого необходимо было иметь оба изомера. Однако все имеющиеся препараты являются г аис-формами. Обнаруженная нами ранее [12] примесь г мс-формы в препарате феруловой кислоты оказалась следствием ее изомеризации на свету. Такое положение наблюдается и в отношении других оксикоричных кислот - кофейной и тг-кумаровой. [41]
Как видно из данных табл. 1, только облученная УФ-светом феруловая кислота вызывает усиление роста. Получение некоторого стимулирующего эффекта и при работе с транс-формой ( необлученной) является следствием ее изомеризации в водных растворах, особенно на свету. Кроме того, в опытах с длительной экспозицией ( с прорастанием семян, с инфильтрацией) возможна ферментативная изомеризация т сшс-феруловой кислоты в тканях за счет цис-транс-язомераз. Правда, изомеразы коричных кислот еще не известны, но г мс-г гшс-изомераза малеиновой - фумаро-вой кислот обнаружена в бактериях. Следовательно, и природный представитель оксикоричных кислот - феруловая кислота-проявляет ростовое действие в зависимости от геометрической структуры: цис-форыа. [42]
Страницы: 1 2 3