Фуранкарбоновая кислота
Cтраница 3
Фуриловый альдегид ( фурфурол) обнаруживает все свойства ароматического альдегида. Подобно бензальдегиду, он превращается по реакциям Канницарро в фуриловый спирт и фуранкарбоновую кислоту, дает с ацетатом натрия и уксусным ангидридом ( по реакции Перкина) аналог коричной кислоты-фурилакриловую кислоту, с цианистым калием уплотняется в аналог бензоина-фуроин. [31]
Фурнловый альдегид ( фурфурол) обнаруживает все свойства аро мгмнческого альдегида. Подобно бензальдегиду, он превращается но реакциям Канницарро в фуриловый спирт и фуранкарбоновую кислоту, дает с ацетатом натрия и уксусным ангидридом ( по реакции Перкина) аналог коричной кислоты-фурнлакриловую кислоту, с цианистым калием уплотняется в аналог бензоина-фуроин. [32]
Виниловые эфиры фуранового ряда относительно мало изучены. В связи с этим нами исследовано взаимодействие ацетилена с 5 - замещенными фурфу-риловыми спиртами и некоторыми фуранкарбоновыми кислотами. Следует подчеркнуть, что реакция идет в аномально мягких условиях, что объясняется своеобразным воздействием фу-рильного радикала. Это особенно заметно, если сравнить с условиями винили-рования тетрагидрофурфурилового, бензилового и аллилового спиртов. [33]
В качающийся автоклав емкостью 150 мл-помещают 23 0 г ( 0 1 моля) метилового эфира 5-п-толилме - тил-2 - фуранкарбоновой кислоты ( см. Синтезы гетероциклических соединений, вып. После удаления воздуха из автоклава его заполняют водородом до давления 100 атм, включают качание и поднимают температуру до 180 ( прим. [34]
Получаемые при этом результаты, приведенные в табл. 14, выявляют сравнительно небольшое различие скоростей реакции пли энергии активации для различных исходных кислот, несмотря на то, что в фуранкарбоновых кислотах проявляется резонанс между карбоксильной и фурановой группами, в то время как в фурануксусных кислотах такой резонанс отсутствует. Поскольку известно, что при других реакциях, например этери-фикации, сказывается влияние резонанса, можно считать вероятным, что в адсорбированном комплексе на поверхности катализатора сопряжение карбоксильной и фурановой групп исчезает. [35]
В круглодонную колбу А емкостью 200 мл через боковой тубус вставлен термометр Б, доходящий почти до дна колбы. Горло колбы А плотно закрыто резиновой пробкой, через которую проходит вертикальная трубка В длиной 15 см и диаметром 1 8 - 2 0 см. Верхнее отверстие трубки В закрывают резиновой пробкой, в которую вставлена длинная стеклянная палочка Г, служащая для сбрасывания в колбу возгоняющейся фуранкарбоновой кислоты. [36]
Гидрирование проведено в присутствии платиновой черни, коллоидного раствора платины, палладия на сернокислом барии и коллоидного раствора палладия. Применялись следующие производные фу-рана: 1) содержащие группу - СН2 - или - СН в - положении фуранового ядра ( фурфурэтилен, фурилакриловая кислота, фуриловый спирт и др.); 2) содержащие группу - СО - в - положении фуранового ядра ( фурилметилкетон, фурилфенилкетон и др.); 3) фурфурол и его производные; 4) фуранкарбоновая кислота и ее производные. Получены следующие данные: представители первой группы гидрируются наиболее легко, затем идет вторая группа, а производные кар-боновых кислот гидрируются с трудом. [37]
Аналогично обработанный а-метилфуран превращается в левули-новый альдегид, а 2 5-диметилфуран - в ацетонилацетон. Эти реакции размыкания фуранового цикла ( а также и описанные ниже реакции) сопровождаются глубоким осмолением. Фуранкарбоновые кислоты и нитрофураны значительно устойчивее к кислотам, чем фуран и его гомологи; фурфурол занимает промежуточное положение. [38]
Полученный таким путем р-нитрофуран ( II) отличается от продукта прямого нитрования фурана. Так как оба а-положения, как и оба - положения, эквивалентны, то этим подтверждается структура соединения, полученного при прямом нитровании. При нитровании фуранкарбоновых кислот часто протекает декарбоксилирование. [39]
Различные метилфуранкарбоно-вые кислоты в большинстве случаев могут быть получены с помощью уже рассмотренных выше методов, среди которых синтезы Фейста-Бенари, вероятно, являются наиболее применимыми. Поэтому подробного рассмотрения этих соединений дано не будет. Из других гомологов фуранкарбоновых кислот заслуживают обсуждения те, в которых карбоксильная группа ( или группы) отделена от ядра одним или большим числом углеродных атомов. [40]
При гидрировании бензонитрила, о - и р-толунитрила в уксусном ангидриде образуются ацетильные производные соответствующих первичных ами-х нов, вторичные амины не образуются; путем омыления продуктов восстановления концентрированной соляной кислотой получаются с хорошим выходом первичные амины. Восстановление бензилцианида протекает медленнее и требует больше катализатора. Триметилцианид, нитрил фуранкарбоновой кислоты и имидазолацетонитрил гидрируются еще медленнее. В качестве побочной реакции имеет место дальнейшее восстановление ацетилированного амина в ацетамид и углеводород. [41]
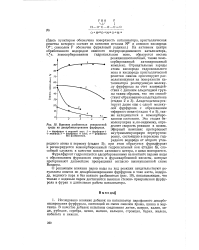 |
Влияние разбавителя реакционной среды на декарбонилирование фурфурола. [42] |
Альдегидатион реагирует далее еще с одной молекулой фурфурола с образованием эфирного иона ( стадии 4 и 5), также находящегося в хемосорбированном состоянии. Эта стадия би-молекулярна и, по-видимому, определяет скорость реакции в целом. Эфирный комплекс претерпевает внутримолекулярную перегруппировку, состоящую в перескоке гид-ридного водорбда от второго углеродного атома к первому ( стадия 5); при этом образуется фурилфуроат и регенерируется хемосорбированньщ гидроксильный ион ( стадия 6), способный служить в качестве нового активного центра, и цикл повторяется. Фурилфуроат гидролизуется адсорбированными на контакте парами воды с образованием фурилового спирта и фуранкарбоновой кислоты, которые претерпевают дальнейшие превращения согласно вышеуказанной схеме Вандора. [43]
Третичный хлористый бутил образует с бензолом третичные как моно -, так и дибутилбензолы, а третичный хлористый амил - третичные моно - и диа-милбен-золы. С толуолом [36] третичный хлористый бутил образует третичный л-бутилтолуол, а с нафталином - третичные один моно - и два бутилнафталина. Нормальный бромистый пропил реагирует с бензолом и дает продукт, содержащий 88 % изопропилбензола и 12 % н-пропилбензола. Третичный хлористый бутил образует с фенолом третичный л-бутилфенол [37], а с этиловым эфиром фуранкарбоновой кислоты - третичный 5-бутилэтиловый эфир фуранкарбоновой кислоты. Фтористый и хлористый циклогексилы образуют с толуолом л-циклогексилтолуол, а 2-фтороктан с толуолом дает 2-л-октилтолуол. Скорости реакции фторидов, хлоридов, бромидов и иодидов соответствуют порядку перечисления. Это совсем не служит указанием на прочность связи углерод - галоид, так как, повидимому, имеет место обратный порядок; не доказывает это и легкости ионизации, потому что вернее всего, как будет показано ниже, ход реакции не соответствует ионному механизму. Различия в скоростях реакций могут быть отнесены за счет легкости удаления галоидоводорода. Образование фтористого водорода не замедляет реакцию, потому что он является катализатором. Хлористый водород, бромистый водород и йодистый водород имеют точки кипения, повышающиеся в порядке их перечисления, и поэтому их растворимости увеличиваются, а легкость удаления уменьшается в том же порядке. [44]
Третичный хлористый бутил образует с бензолом третичные как моно -, так и дибутилбензолы, а третичный хлористый амил - третичные моно - и диа-милбен-золы. С толуолом [36] третичный хлористый бутил образует третичный л-бутилтолуол, а с нафталином - третичные один моно - и два бутилнафталина. Нормальный бромистый пропил реагирует с бензолом и дает продукт, содержащий 88 % изопропилбензола и 12 % н-пропилбензола. Третичный хлористый бутил образует с фенолом третичный л-бутилфенол [37], а с этиловым эфиром фуранкарбоновой кислоты - третичный 5-бутилэтиловый эфир фуранкарбоновой кислоты. Фтористый и хлористый циклогексилы образуют с толуолом л-циклогексилтолуол, а 2-фтороктан с толуолом дает 2-л-октилтолуол. Скорости реакции фторидов, хлоридов, бромидов и иодидов соответствуют порядку перечисления. Это совсем не служит указанием на прочность связи углерод - галоид, так как, повидимому, имеет место обратный порядок; не доказывает это и легкости ионизации, потому что вернее всего, как будет показано ниже, ход реакции не соответствует ионному механизму. Различия в скоростях реакций могут быть отнесены за счет легкости удаления галоидоводорода. Образование фтористого водорода не замедляет реакцию, потому что он является катализатором. Хлористый водород, бромистый водород и йодистый водород имеют точки кипения, повышающиеся в порядке их перечисления, и поэтому их растворимости увеличиваются, а легкость удаления уменьшается в том же порядке. [45]
Страницы: 1 2 3