Добавка - перекись
Cтраница 2
В обзорной статье [37] было сообщено о высокой эффективности добавок разнообразных перекисей. [16]
Первые теории детонации исходили из известного экспериментального факта, что добавка перекиси уменьшает величину степени сжатия, при которой возникают стуки, и связывали возникновение детонации с взрывным разложением перекисей, образующихся при окислении топлива в камере сгорания двигателя. [17]
Исследованы кинетика и продукты термического распада в вакууме поли-1 1 5-три-гидроиерфторамилакрилата, инициированного добавками перекиси дикумила и хлористого цинка. Наблюдаемое в обоих случаях увеличение скорости распада обусловлено различными причинами. В присутствии перекиси дикумила увеличение скорости распада связано с увеличением количества активных центров в цепи макромолекулы, образующихся при взаимодействии продуктов распада перекиси с полимером. В присутствии хлористого цинка происходит изменение механизма распада поли-1 1 5-тригидропер-фторамилакрилата в сторону увеличения степени разрушения сложноэфирных групп, что приводит к снижению термической стабильности полимера. [18]
Подобен этому способ американского патента, использующий применение азотной кислоты ( в 35 % HNO3) с добавкой перекиси марганца. [19]
Ауфрехта на метанол; - окисление пробы хромовой кислотой; дистиллят дает синюю окраску с диметиланилином и серной кислотой после добавки перекиси свинца. [20]
Свободнорадииальной реакции замещения хлора способствует отсутствие поляризующих катализаторов, освещение прямим солнечным светом или УФ-облуче-пие, а при работе с S03Q3 добавка перекисей. [21]
Возможность радикального механизма была отвергнута, так как в продуктах реакции не было обнаружено ни дифенила, ни фенола и, кроме того, добавки перекисей не влияли на скорость реакции. [22]
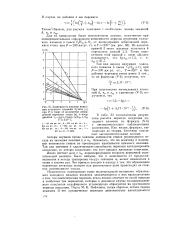 |
Зависимость периода индукции холодного пламени бутана ( TJ ПрИ р const от количества добавленной перекиси этила ( х в координатах tj - Igz. Смесь QH - f - 0 %, Т 320 С. [23] |
Так как период индукции холодного пламени в смеси С4Н10 -) - 02 при / 200 л рт. ст., Т 320 и без добавки перекиси этила равен 5 сек. [24]
При нагревании таких ненасыщенных органических соединений, как акриловая кислота или малеиновый ангидрид, с тетравинил-германием в отсутствие кислорода в течение 18 ч при 50 С с добавками перекиси бензоила образуются сополимеры. [25]
Присоединением брома к чистому нафталину в безводном СС14 при Оа С на свету получают [ 13811 2 3 4-тетрабрам - 112 3 4-тетрагидронафтэлин ( выход 30 %), а в этом же растворителе при комнатной температуре на свету и добавке перекиси ( аскаридол) ( 139 ] получается 12 % этого вещества, К антрацену в сероуглероде при Од С бром присоединяется с образованием Э 10-дибром - 9 10-дигидроантрацена [ 129, 1401; из фенан-трена в эфыре [141] или сероуглероде [142] получается 9 10-дибром - 9 10-дигидрофенан-грен. Оба вещества нри нагревании отщепляют бромистый водород и переходят ь 9-бромзамещенлыс. [26]
Причиной того, что источником разветвления большею частью предполагается распад именно органических перекисей, является, во-первых, общеизвестный факт химической неустойчивости этих соединений и, во-вторых, экспериментально доказанное резкое ускорение ( главным образом сокращение или элиминирование периода индукции) процесса окисления углеводородов при добавке перекисей. Таким образом, для авторов перекисных схем вопрос о химической конкретизации элементарных актов, определяющих вырожденно-раз-ветвленный характер окисления, не представляет особых трудностей. Совсем иное разрешение получил бы вопрос о первичном молекулярном продукте газофазного окисления углеводородов, если бы удалось показать, что вырожденное разветвление в этом процессе обусловливается не соединением перекисного характера ( алкилгидроперекисью), а каким-либо другим промежуточным продуктом. Это с несомненностью говорило бы не только о том, что разветвляет не перекись, но и о том, что перекись вовсе не образуется в качестве первичного молекулярного продукта. Ведь если бы перекись являлась таким промежуточным продуктом, то именно она обусловливала бы разветвление, и реакция не нуждалась бы в другом веществе для этого акта. Таким образом, идентификация вещества, реакция которого определяет вырожденное разветвление, является в какой-то мере и установлением природы первичного молекулярного продукта окисления. [27]
Добавка перекиси вместе с действием ультрафиолетового света обеспечивают уже достаточно быстрое образование при окислении метилциклогексана первоначально возникающей перекиси. [28]
Реакцию проводят в техническом диоксане. При использовании чистого ди-оксана необходима добавка перекиси бензоила. [29]
Легко окисляются кислородом воздуха циклические аце-тали гидробензоина и изогидробензоина [43], причем последний с меньшей скоростью, что объясняется трансиодным расположением фенильных групп в этом соединении, создающим своим взаимодействием дополнительное напряжение диокса-ланового кольца. Окисление ацеталей гидробензоина и изогидробензоина ускоряется добавками перекисей ( например, перекиси бензоила), УФ-светом и ингибируется гидрохиноном. Основными продуктами окисления ацеталя гидробензоина являются бензойная кислота, бенз - и ацетальдегиды. [30]
Страницы: 1 2 3 4