Количество - аминокислота
Cтраница 3
Преимущества метода Вильштеттера и Вальдшмидт-Лейтца не ограничивается простотою проведения; он позволяет также определить в гидролизате отдельно количество аминокислот и пептидов. Это оказывается возможным при применении спирта различных концентраций. [31]
Для количественного определения содержания аминокислот в анализируемой смеси строится калибровочная кривая зависимости площади пятна ( мм2) от количества аминокислоты ( г), используемой в качестве свидетеля. Между количеством аминокислоты и площадью пятна на пластинке должна существовать зависимость, выражаемая прямой, выходящей из начала координат. [32]
Из таблиц следует, что количества оксиаминокислот, полученные по методу Фишера, обычно являются только небольшой фракцией того количества аминокислоты, которая определена методом окисления. Они скорее служат доказательством присутствия исследуемой аминокислоты в белке. [33]
Во фракции пасоки, собранной с 17 до 21 ч, остается лишь немного аминокислот, а в пасоке, собранной за ночные часы, количество аминокислот так мало, что их нельзя обнаружить данным методом. Утром 2-го дня плача в пасоке вновь имеется большой набор аминокислот, количество которых уменьшается к вечеру. [34]
Определяя масс-спектрографически соотношение между меченой и немеченой аминокислотой в чистой выделенной аминокислоте и зная количество меченой аминокислоты, введенное в исходную смесь аминокислот, можно вычислить количество немеченой аминокислоты в смеси. Этот метод трудоемок, так как он требует синтеза большого числа меченых аминокислот. [35]
Из краткого изложения исследований, проведенных по механизму сорбции аминокислот, видно, что существуют две точки зрения на процесс сорбции аминокислот, причем большинство исследователей считает, что все сорбированное количество аминокислоты находится в ионите в виде противоионов. [36]
С-Концевая аминокислотная последовательность определяется следующим образом: субстрат инкубируется с ферментом при 25 - 37 Си через определенные интервалы времени из реакционной смеси отбираются ал и квотные части, реакция останавливается подкислением и количество отщепленных аминокислот определяется на аминокислотном анализаторе. [37]
С другой стороны, аспарагиновая и особенно глутаминовая кислоты, а также лейцин, изолейцин и пролии обычно находятся в белках семян растений в количествах более 5 - 8 %, и часто общее содержание этих пяти аминокислот составляет 60 - 70 % количества аминокислот в белках растений. [38]
Для микробиологического получения аминокислот используют способность различных культур ауксотрофных мутантов синтезировать определенную аминокислоту, например глутаминовую или лизин. Количество аминокислот, производимых клеткой, в 10 - 100 раз превышает их расход на построение самих клеток. Эти аминокислоты выделяются в окружающую среду. [39]
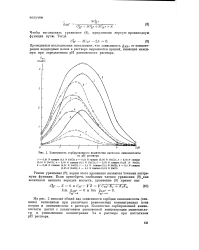 |
Зависимость сорбированного количества катионов аминокислоты. [40] |
На рис. 2 показан общий вид зависимости сорбции аминокислоты ( глицина) катионитом при различных равновесных концентрациях иона натрия и аминокислоты в растворе. Количество сорбированной аминокислоты растет с увеличением равновесной концентрации аминокислоты и уменьшением концентрации Na в растворе при постоянном рН раствора. [41]
Как видно из схемы, всосавшиеся аминокислоты в первую очередь используются в качестве строительного материала для синтеза специфических тканевых белков, ферментов, гормонов и других биологически активных соединений. Некоторое количество аминокислот подвергается распаду с образованием конечных продуктов белкового обмена ( СО2, Н2О и NH3) и освобождением энергии. Это количество составляет около 10 % от суточной потребности организма человека в энергии. Количество аминокислот, подвергающихся распаду, зависит как от характера питания, так и от физиологического состояния организма. Например, даже при полном голодании или частичном белковом голодании с мочой постоянно выделяется небольшое количество азотистых веществ, что свидетельствует о непрерывности процессов распада белков тела. [42]
Для количественного определения содержания аминокислот в анализируемой смеси строится калибровочная кривая зависимости площади пятна ( мм2) от количества аминокислоты ( г), используемой в качестве свидетеля. Между количеством аминокислоты и площадью пятна на пластинке должна существовать зависимость, выражаемая прямой, выходящей из начала координат. [43]
Диапазон изменения количества аминокислоты должен охватывать ожидаемое содержание ее в исследуемом веществе. Затем проводят все операции по хроматографированию, проявлению, экстракции и коло-риметрированию исследуемой аминокислоты. На основании полученных данных строят кривую зависимости между количеством кислоты и изменением оптических свойств ее растворов, окрашенных проявителем. [44]
Данные таблицы 4 показывают, что в почках опытных растений содержание общего и белкового азота на 10-ый день после дефолиации несколько увеличилось. Несколько повышается и количество аминокислот. [45]
Страницы: 1 2 3 4