Количество - адсорбированное вещество
Cтраница 3
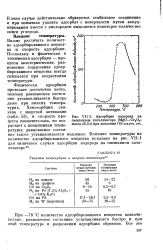 |
I. Адсорбция водорода на смешанном катализаторе ( MgO - Сг2О3. масса 46 5 г при давлении 165 ммрт. cm. [31] |
Важно различать количество адсорбированного вещества и скорость адсорбции. Поскольку и физическая и химическая адсорбция - процессы экзотермические, равновесное содержание адсорбированного вещества всегда снижается при возрастании температуры. [32]
 |
I. Адсорбция водорода на смешанном катализаторе ( MgO - Сг2О3. масса 46 5г при давлении 165 ммрт. ст. [33] |
Важно различать количество адсорбированного вещества и скорость адсорбции. Поскольку и физическая и химическая адсорбция - процессы экзотермические равновесное содержание адсорбированного вещества всегда снижается при возрастании температуры. [34]
 |
Адсорбция водорода на смешанном катализаторе ( MgO-СгаОз. масса 4Q 5 г при давлении 165 мм рт. ст. [35] |
Важно различать количество адсорбированного вещества и скорость адсорбции. Поскольку и физическая и химическая адсорбция-процессы экзотермические, равновесное содержание адсорбированного вещества всегда снижается при возрастании температуры. [36]
Гт - количество адсорбированного вещества ( моль / г адсорбента) на частицах, покрытых плотным монослоем ( емкость монослоя); Р - давление насыщенного пара; В - константа равновесия для полимолекулярной адсорбции, аналогичная константе равновесия в известном уравнении Лэнгмюра [162], описывающем монрмолекулярную адсорбцию. [37]
 |
Адсорбция водорода на смешанном катализаторе ( MgO-СгаОз. масса 46 5 г йри давлении 165 мм рт. ст. [38] |
Важно различать количество адсорбированного вещества и скорость адсорбции. Поскольку и физическая и химическая адсорбция-процессы экзотермические, равновесное содержание адсорбированного вещества всегда снижается при возрастании температуры. [39]
А - количество адсорбированного вещества на единицу массы ( 1 г) адсорбента; с - концентрация раствора в равновесии с адсорбентом; К и п - постоянные для данных веществ: адсорбента, растворителя и растворенного вещества. [40]
СА означает количество адсорбированного вещества ( на грамм или миллилитр адсорбента), a CR - концентрация вещества в растворе. [41]
 |
Изотермы ад. [42] |
Гравн - количество адсорбированного вещества, отвечающее равновесию при данных условиях; Г т - количество вещества, адсорбированного ко времени т; К - коэффициент. [43]
Для определения количества адсорбированного вещества необходимо экспериментально найти давление таза или концентрацию адсорбтива в сосуде, в котором происходит адсорбция, до и после адсорбции. Очень часто количество адсорбированного вещества определяют по привесу адсорбента. Следует заметить, что определение количества адсорбированного вещества вызывает часто большие трудности, всегда имеющие место, когда малая искомая величина является разностью двух больших измеряемых величин. Чтобы уменьшить ошибку измерений, определение обычно проводят, применяя в качестве адсорбента пористые тела с большой удельной поверхностью, связывающие поэтому большое количество адсорбтива. Однако это в свою очередь имеет тот недостаток, что на адсорбции может сказываться диаметр пор адсорбента. [44]
С ростом количества адсорбированного вещества увеличивается площадь, занятая адсорбатом, и уменьшается доля поверхности, способной адсорбировать новые молекулы газа, в результате наблюдается уменьшение величины коэффициента прилипания. Более сложный процесс химической адсорбции ( хемосорбции) определяется не только прямым столкновением молекул газа с атомами поверхности. Хемосорбирующаяся молекула газа при столкновении сначала слабо связывается с поверхностью ( можно считать, что этот процесс соответствует физической адсорбции), а затем перемещается по поверхности, пока не попадет на свободный хемосорбционный центр. Поэ-тому при химической адсорбции коэффициент прилипания не зависит от степени заполнения поверхности. [45]
Страницы: 1 2 3 4