Количество - реагирующее вещество
Cтраница 2
В случае, если количества реагирующих веществ не соответствуют отношению стехиометрических коэффициентов в уравнении реакции, расчет необходимо проводить по тому веществу, которое находится в недостатке и первым заканчивается в результате реакции. При определении избытка-недостатка необходимо учитывать коэффициенты в уравнении реакции. [16]
Обозначения и способ учета количеств реагирующих веществ в уравнении отличаются от цитируемого первоисточника [60] и приняты применительно к настоящей работе. [17]
В результате этой операции получаем количество реагирующего вещества в единицу времени на единицу площади поверхности катализатора. [18]
Скорость химической реакции определяется изменением количества реагирующих веществ ( исходных или конечных) в единицу времени. [19]
Количество катализатора по сравнению с количеством реагирующих веществ незначительно. [20]
За скорость химической реакции принимают изменение количества реагирующего вещества ( или продукта) во времени в единице объема реакционной системы. [21]
Скорость химической реакции определяют как уменьшение количества реагирующего вещества или как увеличение количества продукта за единицу времени, например за секунду. Для реакций, протекающих при постоянном объеме, как например в закрытом сосуде или в растворе, скорость выражают через уменьшение концентрации реагирующего вещества или увеличение концентрации продукта, отнесенных к единице времени. [22]
Скорость прямой реакции по мере уменьшения количеств реагирующих веществ будет постепенно уменьшаться, а скорость обратной реакции по мере увеличения количеств образующихся NaHSO4 и НС1 будет увеличиваться, пока не наступит такой момент, при котором скорости прямой и обратной реакций сделаются равными и установится подвижное, или химическое, равновесие. При химическом равновесии не прекращаются ни прямая, ни обратная реакции, но сколько молекул взаимодействующих веществ в единицу времени превращается в продукты реакции, столько же молекул этих веществ образуется в результате обратной реакции. [23]
Эта величина, очевидно, равна количеству реагирующего вещества, отнесенному к единице наружной поверхности зерен, деленному на пористость катализатора. [24]
Величина Go, очевидно, равна количеству реагирующего вещества, отнесенному к единице наружной поверхности зерен, деленному на долю свободного объема внутри зерен катализатора. [25]
Величина G0, очевидно, равна количеству реагирующего вещества, отнесенному к единице наружной поверхности зерен, деленному на долю свободного объема внутри зерен катализатора. [26]
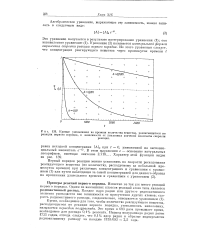 |
Кривые уменьшения во времени количества вещества, разлагающегося по реакции первого порядка, в зависимости от указанных значений константы скорости. [27] |
Время, необходимое для того, чтобы количество реагирующего вещества, распадающегося по реакции первого порядка, уменьшилось наполовину, называется периодом полураспада. Это время в 693 раза превышает время, необходимое для распада 0 1 % реагента. Период полураспада радия равен 1733 годам, отсюда следует, что 0 1 % ядер радия в образце подвергаются радиоактивному распаду за каждые 1733 / 693 2 5 года. [28]
Время, необходимое для того, чтобы количество реагирующего вещества, распадающегося по реакции первого порядка, уменьшилось наполовину, называется периодом полураспада. Это время в 693 раза превышает время, необходимое для распада 0 1 % реагента. Период полураспада радия равен 1733 годам, отсюда следует, что 0 1 % ядер радия в образце подвергается радиоактивному распаду за каждые 1733 / 693 2 5 года. [29]
Количественный метод в химии опирается на точное определение количеств реагирующих веществ, на измерения их масс. Как составление химических формул и уравнений, так и все описанные нами в дальнейшем работы, связанные с атомными весами, были бы невозможны, если бы не был известен важнейший физико-химический закон, закон сохранения массы. [30]
Страницы: 1 2 3 4