Количество - сорбированное вещество
Cтраница 1
А - количество сорбированного вещества; А - предельная адсорбция; С - равновесная концентрация вещества; b - постоянная. [1]
При этом количество сорбированного вещества пропорционально его парциальному давлению. [2]
 |
Количество влаги, поглощенной.| Схемы установок для осушки природного газа. [3] |
А - количество сорбированного вещества за время Т ( рис. 20), то можно видеть, что процесс адсорбции в слое адсорбента включает две стадии: первую стадию - до проскока и вторую - до максимального поглощения паров воды. [4]
Под а мы понимаем сумму количеств сорбированного вещества и свободного газа, находящихся а в единице объема. [5]
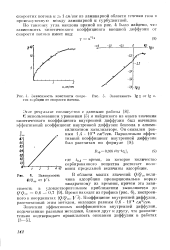 |
Зависимость константы скоро - [ IMAGE ] 5. Зависимость lg у от lg и. сти сорбции от скорости потока. [6] |
Де о 5 - время, за которое количество сорбированного вещества достигает половины предельной величины адсорбции. [7]
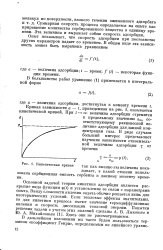 |
Кинетическая кривая так как именно эта величина показывает, в какой степени использована сорбционная емкость сорбента к данному моменту времени. [8] |
Суммарная скорость процесса определяется на опыте как приращение количества сорбированного вещества в единицу времени. Эта величина и выражает собою скорость адсорбции. [9]
Вопрос о связи между размерами зоны Хроматограммы и количеством сорбированного вещества, расположенного в ней, был впервые поставлен М. С. Цветом [1], отмечавшим отсутствие пропорциональной зависимости вследствие неодинаковой степени насыщения по высоте зоны. Исследуя различные виды хроматографического анализа, к этому же выводу приходят и другие исследователи. Так, М. А. Константинова-Шлезингер и Н. А. Горбачева [63] указывают на невозможность использования этой зависимости в сорб-ционной хроматограмме. Они считают метод нецелесообразным и для одного вещества, так как нет пропорциональной зависимости даже при больших концентрациях. [10]
Форма пика, его высота и площадь связаны с количеством сорбированного вещества и служат основой для определения изотерм сорбции, поверхности адсорбента и ряда других характеристик. [11]
 |
Изотермы адсорбции в статических условиях. [12] |
Из уравнения следует, что при повышении концентрации раствора или парциального давления газа возрастает количество сорбированного вещества. При этом устанавливается зависящее от температуры равновесие между числом сорбирующихся и десорби-рующихся молекул в единицу времени. [13]
Здесь ц - химический потенциал адсорбата [ iRTln ( p / ps) ]; Na - количество сорбированного вещества; Т - температура; индексы и - обозначают соответственно адсорбционную и десорб-ционную ветви изотермы; индекс о относится к состоянию на обратимом участке изотермы до точки начала гистерезиса; индекс s относится к состоянию, равновесному насыщенному пару адсорбтива; для мезопористых адсорбентов это, как правило, состояние полного насыщения пространства пор. [14]
Газы при температуре выше критической не взаимодействуют или взаимодействуют в очень небольшой степени с органическими твердыми полимерами и количество сорбированного вещества является незначительным, вследствие чего структура твердого полимера не испытывает каких-либо напряжений вследствие набухания и не подвергается перестройке. Следовательно, растворимость, коэффициенты диффузии и проницаемости оказываются постоянными и не зависят от давления при любой данной температуре. С другой стороны, процессы сорбции и диффузии более легко конденсируемых паров часто в заметной степени зависят от концентрации сорбируемого вещества. Сильные растворители вызывают набухание и пластифицируют полимер, приводя к повышению подвижности сегментов полимера и молекул сорбированного вещества. [15]
Страницы: 1 2 3