Количество - сорбированное вещество
Cтраница 2
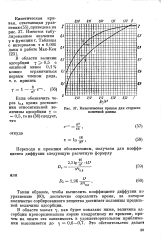 |
Кинетическая кривая для стержня конечной длины. [16] |
Таким образом, чтобы вычислить коэффициент диффузии по уравнению ( 60), достаточно определить время, за которое количество сорбированного вещества достигает половины предельной величины адсорбции. [17]
В отмеченных условиях скорость десорбции определяется главным образом скоростью внутренней диффузии. По мере уменьшения количества сорбированного вещества скорость десорбции сильно замедляется, что объясняется, с одной стороны, уменьшением коэффициента диффузии и, с другой стороны, уменьшением градиента концентрации в адсорбированной фазе. [18]
 |
Распределение концентраций компонентов в газовой фазе по высоте слоя цеолита NaX. [19] |
В отмеченных условиях скорость десорбции определяется главным образом скоростью внутренней диффузии. По мере уменьшения количества сорбированного вещества скорость десорбции сильно замедляется, что объясняется, с одной стороны, уменьшением коэффициента диффузии и, с другой стороны, уменьшением градиента концентрации в адсорбционной фазе. [20]
 |
Схема отбора чистых веществ при неполном разделении их смеси. [21] |
Ширина хроматографического пика может служить мерой кинетических явлений, так как она связана с размыванием хроматогра-фической зоны, которое определяется эффективным коэффициентом диффузии. Наконец, с количеством сорбированного вещества связаны высота и площадь пика, вследствие чего эти величины могут служить основой для определения изотерм сорбции, поверхности сорбента и ряда других сорбционных характеристик. [22]
Имеются определенные ограничения в требованиях к изотермам при рассмотрении закономерностей динамики ионного обмена. Напомним, что вся аналитическая хроматография базируется на линейных зависимостях между количеством сорбированного вещества и его концентрацией в растворе в условиях равновесия. При этом одним из центральных вопросов является анализ вида кривизны - знака второй производной от сорбционной емкости по концентрации вещества во внешнем растворе. Все это говорит о том, что при разработке препаративных динамических процессов также целесообразно использовать определенные разумные ограничения по отношению к точности аналитического описания изотерм вонного обмена. [23]
В связи с этим предварительное изучение сорбции рекомендуется проводить не только на измельченных навесках породы, но и на монолитных образцах ее с помощью так называемого балансового метода. Проводя аналогичные опыты на монолите при других начальных концентрациях раствора С0 и определяя соответствующие им количества сорбированного вещества, можно построить график N ( CP) и определить характер и параметры изотермы сорбции. Здесь, как и ранее, N - количество поглощенного вещества, отнесенное к единице порового пространства; Ср - равновесная концентрация вещества в растворе. [24]
К их числу относятся массовый метод, основанный на определении равновесного количества сорбированного вещества по изменению массы сорбента, и объемный, принцип которого заключается в определении количества сорбированного вещества по разности между числом молей пара, находящегося в известном объеме до и после сорбции. [25]
Ширина хроматографического пика может служить мерой кинетических явлений, так как она связана с размыванием хромато-графической зоны. Последнее определяется эффективным коэффициентом диффузии. Наконец, с количеством сорбированного вещества связаны высота и площадь пика, вследствие чего эти величины могут служить основой для определения изотерм сорбции, поверхности адсорбента и ряда других сорбционных характеристик. [26]
Условия 1 и 3 выполняются для многих адсорбционных систем, в то время как условие 4 соблюдается редко. Количество растворенного вещества, которое адсорбируется в процессе однократного распределения, обычно изменяется с изменением концентрации этого вещества в дробной степени. В этом случае зависимость количества сорбированного вещества от его исходной концентрации нелинейна и изображается кривой. В результате получаются несимметричные зоны, имеющие растянутый фронт или растянутую хвостовую часть; такие зоны перекрываются. На рис. 14.3 схематически показано влияние формы кривой распределения на форму элюируемой зоны. [27]
В этом случае вначале работают по вышеуказанному методу, декантируют раствор, добавляют щелочь для растворения смолы, разбавляют, осаждают НС1 и промывают. Этот метод точнее, так как он уменьшает количество сорбированных веществ. [28]
 |
Кривая сорбции ацетона ( я и пиридина ( б нитроцеллюлозой.| Aw ( в делениях интерферометра для смеси пиридин-петролейвый эфир. [29] |
Если данные по теплотам сорбции представить в виде диаграмм ( рис. 3), то мы получим приблизительно прямую линию. Точки для системы ацетон - петролейный эфир несколько отклоняются от прямой, причем это объясняется некоторым понижением величины теплот ( при измерениях) благодаря сильной растянутости процесса взаимодействия нитроцеллюлозы со смесью ацетон - петролейный эфир при низких концентрациях ацетона. В целом можно считать, что истинная теплота сорбции растворителя нитроцеллюлозой прямо пропорциональна количеству сорбированного вещества. [30]
Страницы: 1 2 3