Добавление - электрон
Cтраница 4
Следует отметить, что максимальное значение электронной концентрации для каждого структурного типа во всех системах примерно одинаково. Это позволяет предположить, что для заполнения энергетической зоны имеется вполне определенное число разрешенных состояний. Такое положение в свою очередь может быть непосредственно связано с определенными размерами зоны Бриллюэна и дает основание считать, что при добавлении электронов будет образовываться новая структура. [46]
Ион Sn4 имеет промежуточное значение радиуса, равное 0 71, в то время как радиус Zr4 равен 0 79 А. Приемлемое объяснение такой неожиданной близости радиусов для членов 4d - и 5d ce - мейств обычно дают, учитывая природу и число добавленных электронов и тот факт, что заселяется только один квантовый уровень. Таким образом, при переходе от Ti4 к Zr4 число электронов увеличивается на 18, из которых 10 -слабо экранирующие ( i-электроны; при этом добавление электронов на новый квантовый уровень вызывает небольшое увеличение размеров. [47]
 |
Разрезы моделей s -, p - и d - орбиталей. Черная точка обозначает атомное ядро. [48] |
Для построения моделей многоэлектронных атомов набор всевозможных ( исходя из допустимых сочетаний значений квантовых чисел) атомных одноэлектронных орбиталей располагается в ряд в порядке возрастающих значений соответствующих им энергетических уровней. Затем в этом же порядке на эти орбитали помещают характерное для данного атома количество электронов. Чтобы учесть взаимодействие электронов, уменьшают эффективный заряд ядра в выражении для соответствующей одноэлектронной орбитали водородоподобного атома, вычитая из заряда так называемую константу экранирования, зависящую от количества электронов, размещенных до добавления данного электрона. [49]
При подходе к химической связи в рамках метода валентных связей ( ВС) предполагается, что электроны на атомных орбиталях ( часто гибридных) перекрываются с образованием связей. Метод молекулярных орбиталей рассматривает ядра всей молекулы как одно полицентрическое ядро и строит систему молекулярных орбиталей, характеризуемых наборами квантовых чисел, подобно тому, как строятся атомные орбитали в атомах. После построения системы МО добавляются электроны, причем соблюдаются условия, накладываемые принципом Паули. При добавлении электронов сперва занимаются орбитали с более низкими энергиями и учитывается правило Гунда. Часто вводят приближенное предположение о том, что молекулярные орбитали могут быть представлены в виде линейных комбинаций атомных орбиталей. Такое приближение обозначается буквами ЛК. Для того чтобы атомные орбитали могли взаимодействовать с образованием молекулярных орбиталей, они должны, во-первых, иметь близкие энергии, во-вторых, перекрываться в заметной степени и, в-третьих, иметь одинаковую симметрию относительно линии связи в молекуле. [50]
Разрыхляющие молекулярные орбитали отмечают звездочками. Заселение их электронами уменьшает энергию и прочность химической связи. Сами электроны на РМО называются разрыхляющими. Для СМО добавление электронов увеличивает энергию связи. Электроны на СМО также называются связывающими. [51]
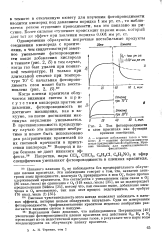 |
Ток фотопроводимости. [52] |
Никакого влияния О2 не наблюдается без предварительного облучения пленки красителя. Эти наблюдения говорят о том, что, захватив электроны зоны проводимости, молекула 02 превращается в ион Oj, более прочно удерживаемый красителем. Вейсса [34], потому что, как сказано выше, добавление электрона к 02 невозможно, так как этот процесс эндотермичен, он требует 176 ккал. [53]
У лантаноидов ( как и у актиноидов) увеличение ат.н. приводит не к повышению, а к понижению размеров атомов и ионов. Причина этого явления, называемого лантаноидным сжатием-неполное экранирование добавочными 4 / электровами уже имеющихся 4 / - электронов. С ростом ат.н. РЗЭ увеличивается эффективный заряд ядра, воздействующий на каждый из / - электронов, а неполное экранирование последних вызывает смещение электронных оболочек атомов ближе к ядру. Это смещение не совсем регулярно, и наиб, выражено при добавлении электронов к / - и / 7-оболочкам. [54]
Поле ядра атома, удерживающее электроны, притягивает также и свободный электрон, если он окажется вблизи атома. Вместе с тем этот электрон испытывает и отталкивание со стороны электронов атома. Теоретический расчет и экспериментальные данные показывают, что для многих атомов энергия притяжения свободного электрона к ядру превышает энергию его отталкивания от электронных оболочек. Атомы могут присоединять электрон, образуя устойчивый отрицательный однозарядный ион. Энергия, выделяющаяся при добавлении электрона к нейтральному атому, который в результате переходит в однозарядный отрицательный ион, называется сродством атома к электрону. Эту величину можно трактовать как взятую с тем же знаком энергию отрыва электрона от отрицательного однозарядного иона. Подобно энергии ионизации сродство к электрону обычно выражают в электронвольтах. [55]
Мы уже часто обращались к периодической системе, или периодической таблице элементов Менделеева ( табл, 1, стр. В периодической таблице элементы расположены по правилам, которые первоначально основывались на их химических свойствах и атомных весах. Поэтому в начале каждого шага мы имеем элемент с известной электронной конфигурацией, затем предполагаем, что заряд ядра этого атома увеличился на единицу и одновременно на периферии электронной оболочки появился еще один электрон. Собственно, мы и хотим узнать, как происходит это добавление электрона. [56]
В простейшем случае атом состоит из центрального ядра, вокруг которого вращаются электроны. Например, водородный атом имеет один электрон, вращающийся вокруг протона. Это -; простейший из всех атомов. Он-имеет два протона и два нейтрона в ядре, вокруг которого вращаются два электрона. Последующие атомы образуются добавлением планетарных электронов и увеличением заряда ядра, вызываемым увеличением в нем числа протонов. При этом нейтроны также должны быть прибавлены к ядру для сохранения стабильности. [57]
Страницы: 1 2 3 4