Комплекс - кобальт
Cтраница 2
Хлорамминные комплексы кобальта ( 111) [ и аналогичные комплексы хрома ( 111) ] отличаются от своих хлоридов не только окраской, но и реакционной способностью. Например, добавление к раствору нитрата серебра свежеприготовленного раствора СоСЬ - бННз приводит к немедленному осаждению всех ионов хлора. Тот же опыт с СоС1з - 5ЫНз показывает, что в этом случае осаждаются только / з ионов хлора; / з ионов осаждается медленно при продолжительном стоянии. [16]
Солянокислый комплекс кобальта с аниони-тами устойчив лишь в сильнокислых средах. Поэтому для его десорбции применяют слабокислые растворы. [17]
Пентадентатные комплексы кобальта с этилендиаминтетра-уксусной кислотой Na [ CoHY ] X, где Y - четырехзарядный анион ЭДТА, X - С1 -, Вг - или J -, были синтезированы в работе [1104]; были изучены также их инфракрасные спектры. [18]
Нитрилопентамминовые комплексы кобальта ( III) иногда получают нитрозированием азидопентамминовых соединений в соответствующем нитриле. В этих реакциях нитрил играет роль растворителя и внедряющегося в комплекс лиганда. [19]
Нерастворимый красно-коричневый комплекс кобальта экстрагируют при рН 1 5 - г - 10 бензолом, четыреххлористым углеродом или другими растворителями и определяют фотометрическим методом при Я 375ч - 380 нм. Растворимый в воде зеленый комплекс железа экстрагируют изоамиловым или бутиловым спиртом и определяют фотометрическим методом при К 700 - s - 710 нм. [20]
Исходный низкоспиновый диметилглиоксиматный комплекс кобальта ( III) инертен; даже в присутствии небольшого избытка диметилглиоксима он образуется количественно, а координированную молекулу диметилглиоксима из комплекса нельзя вытеснить даже большим избытком монодентатного лиганда. В то же время замещение молекул растворителя соответствующими монодентатными лигандами есть процесс обратимый, достигающий равновесия за относительно короткое время. [21]
Некоторые комплексы кобальта ( П) малорастворимы и могут быть легко получены. [22]
Некоторые комплексы кобальта ( II) малорастворимы и могут быть легко получены. [23]
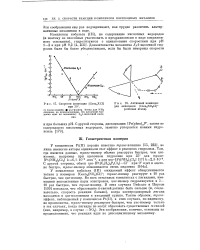 |
Скорости акватации [ Соеп2ХС1 ] при 30.| Активный комплекс. [24] |
У комплексов кобальта ( III) ожидаемый эффект обнаруживается только у изомеров [ Coen2 ( N02) Cl ]; транс-изомер реагирует в 10 раз быстрее, чем zfKc - изомер. Во всех остальных комплексах с лигандами, имеющими неподеленные пары электронов, ис-изомер гидролизуется в 5 - 10 раз быстрее, чем транс-изомер. В этих случаях Бейсоло и Пирсон [199] показали, что образование я-связей должно быть сильнее ( и, следовательно, скорость реакции больше), когда электродонорный лиганд находится в ыс-положении к уходящей группе. Эти соображения, конечно, основаны на предположении, что реакции идут по диссоциативному механизму. [25]
Система комплексов кобальта ( III) является хорошим примером того, что остаточный эффект по существу - небольшая величина не только в системах с менее прочными химическими связями, но также в системах с типичными гомеополярными связями. Бьеррумом, и системы галогенидных комплексов ртути ( II), описанные в литературе. Другой вопрос, всегда ли справедлива точка зрения, высказанная в предыдущей главе, а именно, что остаточный эффект в системах комплексов является в основном малой величиной независимо от природы химической связи. На самом деле было бы весьма естественно, если бы в системах, где центральная группа и лиганды имеют общие электроны, было найдено большее отклонение от чисто статистических условий, чем в системах в основном с электростатическими силами. [26]
Система комплексов кобальта ( III) является хорошим примером того, что остаточный эффект по существу - небольшая величина не только в системах с менее прочными химическими связями, но также в системах с типичными гомеополярными связями. Бьеррумом, и системы галогенидных комплексов ртути ( II), описанные в литературе. Другой вопрос, всегда ли справедлива точка зрения, высказанная в предыдущей главе, а именно, что остаточный эффект в системах комплексов является ъ основном малой величиной независимо от природы химической связи. На самом деле было бы весьма естественно, если бы в системах, где центральная группа и лиганды имеют общие электроны, было найдено большее отклонение от чисто статистических условий, чем в системах в основном с электростатическими силами. [27]
В моноциклопентадиенильных комплексах кобальта способность цикло-пентадиенильного кольца к реакциям замещения зависит от природы другого лиганда, связанного с атомом кобальта. Так, СБН5Со ( СО) 2 разлагается хлористым водородом в условиях ацилирования по Фриделю - Крафтсу с образованием циклопентадиена. [28]
При этом тетратиоцианатный комплекс кобальта ( П) переходит в органическую фазу и окрашивает ее в синий цвет. [29]
Электронные спектры комплексов кобальта ( П) во многих случаях могут дать ценную структурную информацию. Большинство шести-координационных комплексов имеют высокоспиновую электронную конфигурацию. Диаграмма Оргела этих комплексов представлена на рис. 10.11. Основное их состояние - 4Т 9, и спин-орбитальное взаимодействие значительно. Переход 4Tlg ( F) - 4A2g двухэлектронный и не неблюдается. Плечо появляется потому, что спин-орбитальное взаимодействие в возбужденном состоянии 4Т19 ( Р) снимает вырождение. [30]
Страницы: 1 2 3 4