Комплекс - кобальт
Cтраница 3
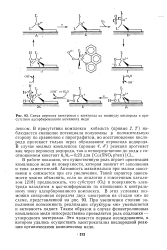 |
Схема переноса электронов с электрода на молекулу кислорода в присутствии адсорбированного комплекса меди. [31] |
В присутствии комплекса кобальта ( кривые 2, 2) наблюдается смещение потенциала полуволны в положительную сторону по сравнению с пирографитом, но восстановление кислорода протекает только через образование пероксида водорода. [32]
Механизм трансформации комплексов кобальта ( П) в ходе окисления этилбензола иной. [33]
При окислении комплекса кобальта ( II) бромом на холоду образуются [3, 4] комплексы кобальта ( III), в которых этилендиамин-тетрауксусная кислота выступает в качестве пятидентатного лиганда; шестое место в координационной сфере металла занимает ион брома. Анион CoYBr2 окрашен в темно-зеленый цвет. Полученные соединения относительно нестойки и легко, особенно при нагревании, отщепляют ион брома. [34]
Для образования комплекса кобальта с ЭДТА прибавляют титрованный раствор последнего в избытке. Затем проводят обратное титрование избытка ЭДТА титрованным раствором соли цинка с эриохром черным Т в качестве индикатора. [35]
При окислении комплекса кобальта ( II) бромом на холоду образуются [3, 4] комплексы кобальта ( III), в которых этилендиамин-тетрауксусная кислота выступает в качестве пятидентатного лиганда; шестое место в координационной сфере металла занимает ион брома. Анион CoYBr2 окрашен в темно-зеленый цвет. Полученные соединения относительно нестойки и легко, особенно при нагревании, отщепляют ион брома. [36]
Как для комплексов кобальта, так и для комплексов марганца в условиях, когда фосфиновые лиганды замещают только одну группу СО, найдено замещение двух карбонильных групп на фосфитные лиганды. [37]
Рентгеноструктурное исследование комплекса кобальта 8.3 показало [20], что атомы углерода ацетиленовой группы находятся между двумя атомами металла, так что каждая из двух ортогональных я-связей ацетилена взаимодействует с одним атомом кобальта. [38]
Спектр поглощения комплекса кобальта, полученного при экстракции ацетилацетоном водного раствора ( рН 1), содержащего 100 мкг / мл элемента, имел максимум све-топоглощения при 420 - 440 нм, что используется для количественного определения кобальта. Влияние кобальта проверяли на серии растворов с различными содержаниями кобальта и хрома. Как и следовало ожидать, присутствие кобальта приводит к завышенной оптической плотности комплекса хрома. [39]
Механизм трансформации комплексов кобальта ( П) в ходе окисления этилбензола иной. [40]
Для образования комплекса кобальта значение рН должно быть 6 - 8, но образовавшийся комплекс устойчив в соляной и азотной кислотах. [41]
Для образования комплекса кобальта с ЭДТА прибавляют титрованный раствор последнего в избытке. Затем проводят обратное титрование избытка ЭДТА титрованным раствором соли цинка с эриохром черным Т в качестве индикатора. [42]
Для образования комплекса кобальта с ЭДТА прибавляют титрованный раствор последнего в избытке. [43]
Максимум светопоглощения комплексом кобальта с 2-нитрозо - 1-нафтолом наблюдается при 360 нм, но при этой длине волны реагент также сильно поглощает свет. Измеряя оптическую плотность при 530 нм, можно снизить до минимума поглощение света реагентом, а содержание свободного реагента в органическом экстракте можно снизить промывкой его разбавленным раствором гидроокиси натрия. [44]
В присутствии Bi3 комплекс кобальта [ Co ( NCS) 4 ] 2 - экстрагируют изоамиловым епир-том, а соединение висмута остается в водном растворе. [45]
Страницы: 1 2 3 4