Комплекс - пиридин
Cтраница 2
Комплексы пиридина с галогенами ( 283) диссоциируют при нагревании; галоген отщепляется так легко, что эти соединения можно использовать как мягкие галогенирующие агенты, например, для фенола и анилина. Комплексы с тригалогенидами бора ( 290) и трехокисью серы ( 291) разлагаются кипящей водой с выделением пиридина. Пиридин-сульфотриоксид является мягким сульфирующим агентом ( см. сульфирование фурана и пиррола, стр. [16]
Непосредственное взаимодействие с бромом может привести к окислению и осмолению фурана. Для бромирования употребляют поэтому комплексы пиридина или диоксана с бромом. Во всех случаях замещаются в первую очередь а-водородные атомы. [17]
Непосредственное взаимодействие с бромом может привести к окислению и осмолению фурана. Для бронирования употребляют поэтому комплексы пиридина или диоксана с бромом. Во всех случаях замещаются в первую очередь а-водородные атомы. [18]
Каталитическая активность пиридина заметно выше в присутствии Со ( П), чем Ni ( II) той же концентрации. Каталитическая волна водорода, вызываемая комплексами пиридина с Со ( П) или Ni ( II), имеет четко выраженный поверхностный характер. [19]
Каталитическая активность пиридина заметно выше в присутствии Со ( П), чем Ni ( II) той же концентрации. Каталитическая волна водорода, вызываемая комплексами пиридина с Со ( П) или Ni ( II), имеет четко выраженный поверхностный характер. [20]
Как показал ряд экспериментальных исследований40 45, предполагаемая схема реализуется при использовании соответствующих комплексообразователей, среди которых Одним из наиболее удобных является хлористый цинк. Так, нагревание до 380 С комплекса пиридина с ZnCl2 в тщательно вакуумированных ампулах приводит к образованию темноокрашенного полимерного вещества. [21]
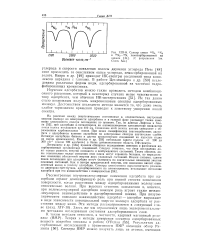 |
Спектр смеси 14N2, I5N2 и Nj - 15N, хемосорбированной на никеле. ( С разрешения Лпг Спет. Soc. [22] |
Квирк и др. [49] приводят ИК-спектры соединений типа комплексов пиридина с глинами. В работе Цетлемойера и др. [50] исследованы различные формы воды, адсорбированной на частично гидро-фобизованных кремнеземах. [23]
Применение пиридина позволяет получить лишь 34 % трис ( триэтилсилил) бората [515], хотя известно, что триалкилбора-ты получаются из треххлористого бора и спиртов в присутствии пиридина с отличным выходом. В ходе реакции в значительных количествах образуются гексаэтилдисилоксан и комплекс пиридина с треххлористым бором. [24]
Наибольший интерес представляет вопрос о структуре бинарного комплекса в случаях, промежуточных между молекулярным и ионным комплексообразованием, и о постепенном изменении этой структуры и формы потенциальной поверхности по мере увеличения энергии взаимодействия. Еще в 1956 г. Барроу [37], изучив ИК-спектры комплексов пиридина с карбоновыми кислотами в СНС13 в области скелетных колебаний пиридинового кольца, пришел к выводу, что взаимодействие с СН3СООН не идет дальше образования молекулярного комплекса, а с СС13СООН и CF3COOH приводит к переходу протона и образованию ионного комплекса. [25]
Наибольший интерес представляет вопрос о структуре бинарного комплекса в случаях, промежуточных между молекулярным и ионным комплексообразованием, и о постепенном изменении этой структуры и формы потенциальной поверхности по мере увеличения энергии взаимодействия. Еще в 1956 г. Барроу [37] г изучив ИК-спектры комплексов пиридина с карбоновымя кислотами в СНС13 в области скелетных колебаний пиридинового кольца, пришел к выводу, что взаимодействие с СН3СООН не идег дальше образования молекулярного комплекса, а с СС13СООН и CFgCOOH приводит к переходу протона и образованию ионного комплекса. [26]
При этом, как утверждают, скорость реакции возрастает в 100 раз по сравнению с реакцией, в которой для окисления применяется комплекс пиридина с СгОз. Возможно, это отчасти объясняется большей растворимостью комплекса 3 5-диметилпиразола с Сг03 и, что гораздо более важно, внутримолекулярным ускорением, вызываемым пиразольными ядрами. [27]
Фенилгидра-зин определялся титрованием фелинговой жидкостью326 в макромасштабе. Комплекс пиридина с ацетатом меди имеет синюю окраску - и конечную точку титрования наблюдают по переходу окраски раствора от желтовато-синей в синевато-зеленую. Эти методы не были испытаны в микромасштабе. [28]
Пиридин - значительно более слабое основание, чем аммиак. Пиридин образует довольно прочные комплексы с теми же ионами металлов, что и аммиак. Известны комплексы пиридина с ионами серебра, меди ( интенсивно синего цвета), никеля, кобальта и др. При образовании подобных комплексов, в отличие от предыдущей группы органических реактивов, не происходит вытеснения ионов водорода. [29]
При нитровании индола этилнитратом в присутствии этилата натрия в эфирном растворе получается 3-нитроиндол. При сульфировании индола комплексом пиридина с SO3 получается 3-сульфокислота. [30]
Страницы: 1 2 3