Комплекс - присоединение - протон
Cтраница 1
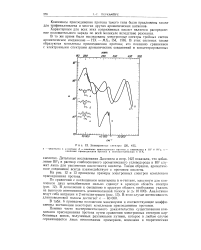 |
Электронные спектры. [1] |
Комплексы присоединения протона такого типа были предложены также для трифенилэтилена и многих других ароматических катионов. [2]
Комплекс присоединения протона, таким образом, представляет собой новую структуру, содержащую СН2 - группу, соседнюю с сопряженной системой. Поскольку атомы водорода связаны с тригональным и тетрагональным атомами углерода, отличающимися по электронной плотности, этот эффект можно наблюдать с помощью спектров ЯМР. [3]
При образовании комплекса присоединения протона четный углеводород превращается в нечетный ион углеводорода. Число л-электронов остается четным, однако в результате образования о-связи оно уменьшается на два. Таким образом получается диамагнитный положительный ион углеводорода. [4]
Четвертой характеристикой комплекса присоединения протона является возникновение положительного заряда. Однако методы, которые могут быть применены в этом случае, непосредственно связаны с термодинамическими соотношениями, поэтому могут служить лишь для анализа систем, присутствующих в растворе. [5]
Как уже говорилось, возможность доказательства образования комплексов присоединения протона с помощью ЯМР-спектроскопии основана на образовании алифатической СН2 - группы. [6]
Спектроскопия ЯМР дает доказательства присутствия в растворе комплексов присоединения протона. [7]
Кроме того, как показали эти исследователи, комплекс присоединения протона к бензолу устойчив только до температуры 220 К - Это, вероятно, является главной причиной, почему существование такого комплекса было доказано лишь недавно. Нестабильность комплекса, а также возможность процессов обмена в растворе, по-видимому, являются также главными причинами, препятствующими наблюдению этого комплекса с помощью ЯМР-спек-троскопии. [8]
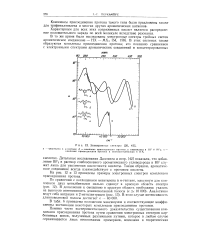 |
Электронные спектры. [9] |
На рис. 12 и 13 приведены примеры электронных спектров комплексов присоединения протона. [10]
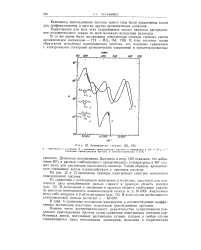 |
Электронные спектры. [11] |
В табл. 6 приведены положения максимумов и соответствующие коэффициенты экстинкции некоторых комплексов присоединения протонов. [12]
Факты, рассмотренные выше, показывают, что для исследования образования комплексов присоединения протона с помощью измерения давления пара необходимо использовать системы с большей кислотностью. [13]
Рассмотренные до сих пор методы определения основности ароматических соединений касались образования комплексов присоединения протона в растворах кислот. Кроме такого взаимодействия известно большое число межмолекулярных взаимодействий, непосредственно связанных с основностью ненасыщенных соединений, в результате которых не происходит образования истинно ковалентных связей. [14]
В предыдущих разделах были рассмотрены экспериментальные и теоретические данные по л-комплексам, EDA-комплексам и комплексам присоединения протона в связи с проблемой основности ненасыщенных я-злектронных систем. Вопросы реакционной способности этих соединений были почти не затронуты, хотя отношение между реакционной способностью и основностью имеет исключительно большое значение для описания механизмов многих реакций. Поскольку недавно был опубликован исчерпывающий обзор по реакции Фри-деля - Крафтса [137], обсуждение ее в настоящей статье не является необходимым. Особое значение имеют обменные процессы Н - D, скорость которых зависит от основности ароматических соединений. Следовательно, существующие методы определения констант основности дополняются кинетическим методом. [15]
Страницы: 1 2 3