Комплекс - родий
Cтраница 1
Комплекс родия имеет состав Rh ( C6H5 - NH CS СНз СЬ. При осаждении из солянокислой среды родий обычно загрязнен иридием. [1]
Комплекс родия регенерируется и готов к новому циклу превращений. [2]
Комплексы родия и иридия очень легко окисляются [ 38а ] перекисью водорода в кислом растворе в соответствующие катионы [ Rh ( С6НБ) 2 ], [ 1г ( С6Н5) 3 ] в которых металл меняет свою формальную степень окисления от - f - 1 до 3, а циклопентадиен теряет атом водорода с образованием ароматического циклопентадиенильного кольца. [3]
Комплексы родия ( 1) в достаточной степени лабильны. [4]
Комплексы родия и иридия очень легко окисляются [ 38а ] перекисью водорода в кислом растворе в соответствующие катионы [ Rh ( С6Н5) 2 ], [ 1г ( С5Н6) 2 ], в которых металл меняет свою формальную степень окисления от - j - 1 до - [ - 3, а циклопентадиен теряет атом водорода с образованием ароматического циклопентадиенильного кольца. [5]
Комплексы родия ( Ш) кинетически инертны, медленно вступают в реакции замещения. Соединения его с галогенид-ионами экстрагируются довольно слабо. [6]
 |
Разрешенная по симметрии тримолекулярная электроциклическая реакция образования металпациклопентана.| Предполагаемый механизм стереоспецифической циклодимеризаци цис - и гранс-пентадиенов. [7] |
Аналогичное циклоприсоединение комплекса родия к соединению, содержащему две ацетиленовые связи, может протекать как согласованный процесс при условии благоприятного пространственного расположения обеих СОсвязей. [8]
В присутствии комплексов родия может также осуществляться и гидрирование альдегидов в спирты. [9]
Для получения правовращающего комплекса родия с ( - основанием в горячий раствор иодида рацемата прибавляют d - тартрат серебра в молярном отношении 2: 3 при постоянном помешивании, без нагревания. Отфильтровав выпавший иодид серебра, выпаривают фильтрат на водяной бане до появления кристаллов, после чего раствор охлаждают. Образуется мелкий кристаллический осадок D-изомера, мало растворимый в холодной воде. Его отфильтровывают, промывают сначала несколькими каплями воды, потом 97 % - ным спиртом. Из 15 г иодида получают 1 25 г кристаллического продукта. [10]
Реакционная способность четырехкоординационных замещенных комплексов родия и иридия типа M ( GO) XLa [ 1096, 1129, ИЗО ] до некоторой степени различна; родиевые производные химически значительно более инертны, чем иридиевые аналоги. Они не проявляют склонности к самопроизвольному окислению, не окисляются также при действии галогенов, не реагируют с растворами кислот и оснований. Соединения мономерны, диамагнитны и не являются электролитами; плавятся с разложением. [11]
Полярограммы восстановления сульфосалицилатных и сульфаминовых комплексов родия имеют три волны с близкими значениями потенциалов полуволн, где третья волна соответствует каталитическому восстановлению ионов водорода. Установлено, что природа предельных токов первой и второй волн носят диффузионный характер. Для суммарной диффузионной двухэлектронной волны был определен коэффициент диффузии, величина которого равна Dn2 6 67 10 6 см2 / с. Из полученных значений угловых коэффициентов и зависимости потенциала полуволны от времени регистрации следует, что восстановление сульфосалицилатных и сульфаминовых комплексов родия ( III) происходит необратимо с замедленны присоединением первого электрона. Эти исследования показали, что с увеличением рН увеличивается доля гидроксокомплексов родия в растворе и скорость электрохимического восстановления комплексов падает. Следовательно, со временем хранения растворов образуются электрохимически более инертные комплексы, может быть полимеризованные, но устойчивые во времени. [12]
Реакция катализируется комплексом родия СЦРРпзЬ Rh ( I), который обозначим для краткости ФМ, где М - металл, Ф - координационная сфера. [13]
Иммобилизованный таким путем комплекс родия, аналогично исходному гомогенному, проявляет высокую каталитическую активность в реакциях гидрирования олефинов. [14]
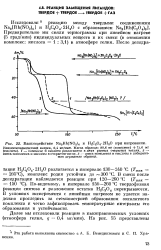 |
Взаимодействие Na3Rh ( NO2 6 и Н2С2О4 - 2Н2О при нагревании. [15] |
Страницы: 1 2 3 4