Комплекс - ртуть
Cтраница 1
 |
Спектр поглощения хлороформного раствора комплекса ртути ( П с дифенилкарбазоном. [1] |
Комплекс ртути ( И) с дифенилкарбазоном при взаимодействии с хлорид-ионами разрушается и интенсивность красной окраски уменьшается. [2]
Однако комплекс ртути не поглощает света при Х436 ммк и потому для определения меди надо только прибавить реактив в количестве достаточном для реакции с обоими этими элементами ( на 1 мг ртути требуется около 2 5 мг диэтилдитиокарбамата. [3]
Некоторые комплексы ртути ( П) уже были упомянуты выше. Ион Hg2 имеет действительно сильную тенденцию к комплексооб-разованию, и для него характерно координационное число два при образовании линейных комплексов и четыре при образовании тетра-эдрических комплексов. [4]
Полагают, что комплексы ртути ( П) в процессе экстракции переходят в органическую фазу в форме гидрато-сольватов ( ме-таллгалогенидные кислоты, гидратно-сольватный механизм экстракции) [306] или сольватов, например LiHgCl3 - S, HgCl2 - 2S, где S - ТБФ, МИБК, ЦГН [299, 1379] и ЩС12 - ТБФ [1387]; эти выводы получены с помощью билогарифмического и ИК-спект-роскопического методов или метода изомолярных серий. В частности, согласно Кузнецову [173], спиртами и кетонами HgCl2 экстрагируется по механизму физического распределения. Не исключено, однако, что HgCl2 образует я-комплексы с бензолом и серу-содержащими экстрагентами. [5]
В работе [27] комплекс ртути с метиленовым зеленым из растворов бромистоводородной и серной кислот в присутствии бромистого калия экстрагируют смесью растворителей; молярный коэффициент погашения составляет 1 105 для растворов бромистоводородной кислоты и 8 104 - для серной кислоты. Линейность калибровочного графика соблюдается для концентраций 0 1 - 2 9 мкг Hg / мл. Определению не мешают 103 - 105-кратные количества Al, Cd, Co, Ni, Mg, Mn, Fe, Cu, Zn, Pb, нитрат -, сульфат - и ар-сенат-ионов. [6]
Хлорид-ионы способны ослаблять окраску комплексов ртути с некоторыми азосоединениями. Закон Вера выполняется в пределах концентрации 0 1 - 4 мкг / мл. [7]
Сравнительно новым является применение вспомогательного комплекса ртути Hg2 с исследуемым комплексоном и связанное с этим использование ртутного электрода. [8]
Так как координационное число исследовавшихся комплексов ртути было равно. Практически все ионы CN -, освобождавшиеся при восстановлении молекул Hg ( CN) 2, при указанных значениях рН превращались в молекулы HCN и диффундировали в раствор. При более высоких рН ионы CN - взаимодействуют с молекулами Hg ( CN) 2 и дают комплексы, более богатые лигандом, что в рассмотренных выше уравнениях не учитывалось. [9]
В этой среде раствор, содержащий комплекс ртути с сульфарсазеном, оранжево-красный; при титровании трилоном Б в точке эквивалентности раствор становится лимонно-желтым. [10]
Для спектрофотометрического определения бромид-ионов рекомендованы смешанные этилендиаминтетраацетат-бромидные комплексы ртути [127], а также бромидные комплексы палладия [402], но методы, в которых они используются, малочувствительны, неспецифичны и довольно сложны. [11]
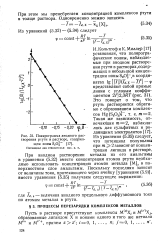 |
Полярограмма анодного растворения ртути в растворе, содержащем ионы S2O - . Потенциал дан относительн нас. к. э. [12] |
При этом мы пренебрегаем концентрацией комплексов ртути в толще раствора. [13]
Таким образом, большая прочность четных комплексов ртути с хлором является проявлением особенности строения электронной оболочки ртути. Судя по - сходству формы кривых для хлоридов, бромидов и йодидов ртути, в последних двух системах следует ожидать такие же соотношения между различными ступенями. [14]
По наблюдению авторов, интенсивность окраски комплексов ртути ( 1) возрастает при стоянии. [15]
Страницы: 1 2 3 4