Комплекс - висмут
Cтраница 2
На рис. 1 представлена кривая светопоглощения раствора тио-мочевинного комплекса висмута; на рис. 2 - праведен калибровочный график для фотометрического определения висмута. [16]
Хлориды, а также бромиды и иодиды разлагают комплекс висмута с ксиленоловым оранжевым. [17]
На рис. 7 приведены кривые светопоглощения ксиленолового оранжевого и комплекса висмута при избытке реактива. На рис. 8 дан калибровочный график для определения висмута с ксиленоловым оранжевым. [18]
В первую очередь титруется В1 1 1 1, так как комплекс висмута Bi - ЭДТА более устойчив, чем комплекс РЬ - ЭДТА. После того как практически весь Bi оттитрован ( первая точка эквивалентности), начинает титроваться РЬ с образованием менее стойкого комплекса РЬ - ЭДТА. При этом оптическая плотность изменяется более резко, так как РЬ - ЭДТА при X 240 нм поглощает значительно сильнее, чем Bi - ЭДТА. [19]
Предскажите форму кривой фотометрического титрования, основанного на этом процессе, зная, что комплекс висмута ( III) с тиомочевяной - единственный компонент системы, поглощающий при выбранной длине волны 465 нм. [20]
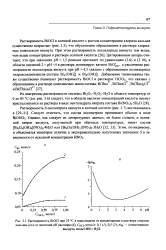 |
Растворимость BiOCl при 25 С в зависимости от концентрации в растворе хлорида кальция ( а и от значений рН раствора ( б, Снсь моль / л. 0 1 ( /, 0 5 ( 2, m & - концентрация. [21] |
Растворимость BiOCl в соляной кислоте с ростом концентрации хлорида кальция существенно возрастает ( рис. 3.5), что обусловлено образованием в растворе хлорид-ных комплексов висмута. [22]
Разработан метод определения Bi в напыленных слоях висмут-селен, содержащих от 1 до 10 % Bi, основанный на ко - лориметрической реакции образования комплекса висмута с тиомочевиной в разбавленном растворе сильной кислоты. [23]
Раствор реагента готовят растворением 2 г 8-оксихинолина в 100 мл воды, содержащей 0 3 мл азотной кислоты; перед употреблением его смешивают с равным объемом 4 % - ного раствора иодида калия. Растворенный комплекс висмута имеет красно-оранжевый или красно-фиолетовый цвет. Коло-риметрирование возможно при содержании от 2 до 100 мг висмута. [24]
Решение вопроса о применении тех или иных соединений при разделении калия, рубидия и цезия зависит от поставленной задачи. Использование комплексов висмута дает возможность обогащать более бедные рубидием концентраты. [25]
Силлен полагает, что существует определенное соответствие между формулами многоядерных комплексов в растворе и кристаллической структурой окислов или основных солей, которые могут быть осаждены из раствора. С этой точки зрения много ядерные комплексы висмута рассматриваются как фрагменты слоев ( ВЮ) П в основных солях висмута. Аналогично ториевые или ураниловые комплексы сходны с фрагментами цепей и слоев, имеющихся в кристаллической структуре основных ( гидроксильных) солей тория и соединений уранила. [26]
Иодидные и тиомочевинные комплексы ЕН3 - иона имеют довольно интенсивную желтую окраску, так что исчезновение этой окраски в результате образования комплекса металла с ЭДТА можно использовать для установления точки эквивалентности. Однако устойчивость и различимость окраски комплексов висмута с обоими индикаторами таковы, что метод опять-таки является недостаточно точным. [27]
Никольс [1010] рекомендует в качестве восстановителя, вместо сернистого газа, раствор сульфата закиси олова. При этом интенсивность окраски от иодидиого комплекса висмута не изменяется, а имеющееся трехвалентное железо восстанавливается до двухвалентного. Другие восстановители будут указаны ниже. [28]
Предложен простой способ определения неизвестных н контроля известных констант нестойкости галогенидных комплексов металлов, основаннный на использовании зависимости констант нестойкости от атомных весов галогенов. Соответствие теоретически найденных констант нестойкости с экспериментальными данными подтверждается примером экстракции хлороформным раствором н-додециламина йодид-ных комплексов висмута. [29]
Разработан экстракционно-фотометрический метод определения висмута, основанный на экстракции трибутил - - фосфатом его комплекса с тиомочевиной из 0 1 - 0 6 М НСЮ4 [145, 146]; определению мешают только Os, Ru, Pd и отчасти Sb и Mo. Интересно, что многие другие изученные органические растворители, в том числе метшгазо-бутилкетон, не извлекают комплекса висмута с тиомочевиной. [30]
Страницы: 1 2 3 4