Комплекс - торий
Cтраница 2
Реакции разрушения сульфат-ионами окрашенного лака тория с амарантом [123], комплекса тория с морином [124], хлоранилата трис - ( 1 10-фенантролината) двухвалентного железа [125], роданид-ного комплекса железа ( III) [60] положены в основу фотометрических методов определения сульфат-ионов. [16]
Разработан спектрофотометрический микрометод определения фторе, основанный на измерении ослабления окраски комплекса тория с арсеназо I в присутствии фторид-иона. Ранее эта реакция была применена для определения малых количеств фтора в неорганических соединениях. [17]
Спектрофотометрическое определение фтора в ЭОС основано на измерении степени ослабления окраски комплекса тория с арсеназо I под действием фторид-иона. [18]
Показана возможность определения до 40 мкг SO по гашению ярко-зеленой флуоресценции моринового комплекса тория в присутствии сульфат-ионов. Флуоресценция стабилизируется через 20 мин и сохраняется в течение нескольких часов. Увеличение температуры снижает флуоресценцию. [19]
Показана возможность определения до 40 мкг SOl по гашению ярко-зеленой флуоресценции моринового комплекса тория в присутствии сульфат-ионов. Флуоресценция стабилизируется через 20 мин и сохраняется в течение нескольких часов. Увеличение температуры снижает флуоресценцию. [20]
При помощи ЭДТА нельзя определить РЗЭ в присутствии тория из-за близких констант устойчивости комплексов тория и тяжелых РЗЭ, а также потому, что комплекс тория с ЭДТА взаимодействует с индикатором ксиленоловым оранжевым с образованием окрашенных соединений. РЗЭ определяют титрованием избытка ДТПА с раствором Pb ( NO3) 2 - Напротив, использование N-оксиэтилен-диаминтриуксусной кислоты ( ОЭДТА) ( V) позволяет определять РЗЭ прямым титрованием. [21]
Большинство констант комплексообразования, приведенных в табл. 2, было измерено посредством регистрации изменений экстрагируемости комплекса тория с ТТА бензолом при введении в водную фазу различных анионов. Поэтому литература, указанная в табл. 2, может быть использована для получения более определенной информации об экстракции тория в присутствии комплексообразующих ионов. [22]
Майорова и Фомин [341] по изменению коэффициента распределения тория при экстракции из нитратных сред трибутил-фосфатом в присутствии сульфат-иона нашли состав и константы устойчивости смешанных нитратосульфатных комплексов тория. [23]
При помощи ЭДТА нельзя определить РЗЭ в присутствии тория из-за близких констант устойчивости комплексов тория и тяжелых РЗЭ, а также потому, что комплекс тория с ЭДТА взаимодействует с индикатором ксиленоловым оранжевым с образованием окрашенных соединений. РЗЭ определяют титрованием избытка ДТПА с раствором Pb ( NO3) 2 - Напротив, использование N-оксиэтилен-диаминтриуксусной кислоты ( ОЭДТА) ( V) позволяет определять РЗЭ прямым титрованием. [24]
Координационное число тория, равное 10, проявляется в его комплексах с бидентатным трополоновым анионом: NaTh ( O2C7H5) 5 и др. Известны также комплексы тория с большим числом других анионов: фталатом, малеинатом, малонатом и пр. [25]
Недавно в практику был введен новый реагент 1 - ( 3 4-дихлорфенил) - 4 4 5 6 6 6-гептафтор - 1 3-гександион, который с торием образует комплекс, значительно более растворимый в бензоле, чем комплекс тория и ТТА. [27]
Найдено [1], что при рН 3 7 окрашенные комплексы тория и редкоземельных элементов ( РЗЭ) с арсеназо различно относятся к нагреванию. Комплекс тория не изменяется, а для комплексов РЗЭ оптическая плотность увеличивается в 1 9 - 2 9 раза при нагревании до 80 С. [28]
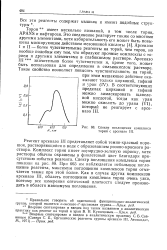 |
Спектр поглощения комплекса тория с арсеназо III. [29] |
Реагент арсеназо III представляет собой темно-красный порошок, растворяющийся в воде с образованием розово-красного раствора. Комплекс тория имеет изумрудно-зеленую окраску, хотя растворы обычно окрашены в фиолетовый цвет благодаря присутствию избытка реагента. При 665 им наблюдается небольшое поглощение реагента, максимум поглощения комплексов тория отмечается также при этой волне. Как в случае других комплексов арсеназо III, область поглощения комплекса тория очень узка, поэтому все измерения оптической плотности следует производить в области максимума поглощения. [30]
Страницы: 1 2 3 4
