Комплекс - желтый цвет
Cтраница 3
Технеций, обладающий более сильными окислительными свойствами, чем рений, восстанавливается роданид-ионами значительно быстрее. В присутствии рения Тс ( VII) почти полностью восстанавливается до более низкога валентного состояния в течение 3 час. Роданид-ионы могут восстанавливать технеций, по-видимому, и до четырехвалентного состояния с образованием комплекса желтого цвета. Однако в органических растворах ( ацетон, эфир) преимущественно образуется комплексное соединение технеция ( V) красного цвета, которое в противоположность комплексу желтого цвета хорошо экстрагируется спиртами, эфирами, кетонами. [31]
Технеций, обладающий более сильными окислительными свойствами, чем рений, восстанавливается роданид-ионами значительно быстрее. В присутствии рения Тс ( VII) почти полностью восстанавливается до более низкого валентного состояния в течение 3 час. Роданид-ионы могут восстанавливать технеций, по-видимому, и до четырехвалентного состояния с образованием комплекса желтого цвета. Однако в органических растворах ( ацетон, эфир) преимущественно образуется комплексное соединение технеция ( V) красного цвета, которое в противоположность комплексу желтого цвета хорошо экстрагируется спиртами, эфирами, кетонами. [32]
Неорганических соединений, имеющих собственную окраску, достаточно интенсивную, чтобы ее можно было использовать для колориметрических определений, немного. Гораздо чаще приходится переводить определяемое бесцветное вещество ( или его ионы) в окрашенное соединение и измерять интенсивность окрашивания полученного раствора. Например, ион меди, имеющий в водном растворе слабую голубую окраску, добавлением аммиака переводят в интенсивно окрашенный комплекс синего цвета. Ион железа ( III) с добавлением сульфосалициловой кислоты в аммиачной среде превращается в комплекс желтого цвета. Раствор солей никеля бледно-зеленого цвета приобретает интенсивное красное окрашивание при введении в него диметилглиоксима в присутствии окислителя. [33]
Основным промежуточным продуктом в производстве металлического титана является его тетрахлорид технический и ректифицированный. Главными примесями четыреххлористого титана, влияющими на качество титановой губки, являются хлориды кремния, ванадия, железа, свободный хлор, фосген и некоторые другие органические соединения. Для определения указанных примесей тетрахлорид титана растворяют в разбавленной азотной кислоте, охлажденной до - 30, - 40, после чего к раствору добавляют серную кислоту и выпаривают до паров се. В дальнейшем ванадий определяют колориметрически с перекисью водорода в присутствии фтор-иона или в виде фосфорновольфрамово-ванадиевого комплекса желтого цвета, который экстрагируют изобутиловым спиртом. Железо определяют колориметрически с роданидом, сульфосалициловой кислотой или с о-фенантролином. Определение кремния осуществляют спектроскопическим методом после растворения тетрахлорида титана в охлажденной до - 30, - 40 разбавленной серной кислоте. Для определения хлора пробу тетрахлорида титана переводят в водный раствор йодистого калия и по количеству выделившегося иода устанавливают количество хлора. Этот метод позволяет определять не только содержание хлора, но и других примесей, способных вытеснять иод из его соединений. Хлор, различные органические хлорпроизводные и другие кислородные органические соединения определяют с помощью инфракрасной спектроскопии. [34]
Для определения Fe2 в воде используют колориметрические методы с 2 2-дипиридилом и о-фенантролином. Сумму Fe3 Fe2 определяют колориметрическим и сульфосалициловым и роданидным методами. Он основан на образовании окрашенных комплексов железа с сульфо-салициловой кислотой или сульфосалициловокислым натрием. В щелочной среде ( рН 8 - 11 5) сульфосалици-ловая кислота реагирует с ионами Fe3 и Fe2, образуя комплекс желтого цвета. Содержание Fe2 находят по разности. [35]
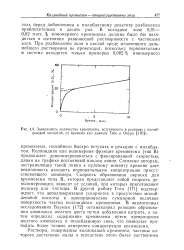 |
Зависимость количества кремнезема, вступившего в реакцию с молибденовой кислотой, от времени ( по данным Гото и Окура. [36] |
Коллоидная или полимерная фракция кремнезема ( тип В) продолжает деполимеризоваться с фиксированной скоростью, давая на графике постоянный наклон линии. Согласно авторам, экстраполяция такой линии к нулевому моменту времени дает возможность находить первоначальную концентрацию присутствовавшего мономера. Скорость образования окраски для кремнезема типа В, которая представляет собой скорость деполимеризации, зависит от условий, при которых приготовляют полимер или частицы. В другой работе Гото [171] подтверждает, что деполимеризация ускоряется в присутствии молибденовой кислоты и пропорциональна суммарной величине поверхности частиц коллоидного кремнезема. В аналогичных исследованиях Бауман [172] останавливал реакцию образования комплекса желтого цвета путем добавления цитрата, а затем определял содержание кремнезема путем превращения желтого комплекса в молибденовую синь, что позволяет проводить более точные измерения концентрации кремнезема. [37]
Рассмотрим возможный ход анализа при выборе меди в качестве коллектора. Соли висмута подвергаются гидролизу значительно лучше солей меди, поэтому при некотором значении рН висмут полностью переходит в осадок вместе с небольшим количеством гидроксида меди. Осадок легко растворяется в кислоте. Однако ионы меди мешают дальнейшему определению ионов висмута в этом растворе. Тем не менее при добавлении тиомочевины ионы меди связываются в бесцветный прочный комплекс, а ионы висмута образуют комплекс желтого цвета. [38]
Технеций, обладающий более сильными окислительными свойствами, чем рений, восстанавливается роданид-ионами значительно быстрее. В присутствии рения Тс ( VII) почти полностью восстанавливается до более низкога валентного состояния в течение 3 час. Роданид-ионы могут восстанавливать технеций, по-видимому, и до четырехвалентного состояния с образованием комплекса желтого цвета. Однако в органических растворах ( ацетон, эфир) преимущественно образуется комплексное соединение технеция ( V) красного цвета, которое в противоположность комплексу желтого цвета хорошо экстрагируется спиртами, эфирами, кетонами. [39]
Технеций, обладающий более сильными окислительными свойствами, чем рений, восстанавливается роданид-ионами значительно быстрее. В присутствии рения Тс ( VII) почти полностью восстанавливается до более низкого валентного состояния в течение 3 час. Роданид-ионы могут восстанавливать технеций, по-видимому, и до четырехвалентного состояния с образованием комплекса желтого цвета. Однако в органических растворах ( ацетон, эфир) преимущественно образуется комплексное соединение технеция ( V) красного цвета, которое в противоположность комплексу желтого цвета хорошо экстрагируется спиртами, эфирами, кетонами. [40]
Страницы: 1 2 3