Комплекс - цинк
Cтраница 3
Ход ASK по ступеням координации для комплексов цинка в основных чертах уже рассмотрен при обсуждении ДЯК. [31]
Поэтому нами применена экстракция изоамиловым спиртом пиридин-роданидного комплекса цинка из нейтральной среды. [32]
Иногда вместо комплексов магния с ЭДТА используют комплекс цинка с ЭДТА. [33]
В аналогичном исследовании установлена большая скорость образования комплекса цинка с ди - ( 1-нафтил) - тиокарба-зоном, почти в 100 раз менее устойчивого, чем комплекс с дитизоном. [34]
 |
Газохроматографиче-ское разделение диэтилдитиофосфи-натов некоторых двухвалентных металлов [ 75а ]. [35] |
Удовлетворительные хроматограммы хелата кадмия ( а также комплексов цинка, никеля, кобальта ( П) и свинца ( П)) были получены на колонках с силиконами SE-30, OV-17 и OV-101 при температурах 200 - 220 С ( рис. VII. В работе приведена калибровочная кривая, согласно которой предел обнаружения хелата кадмия при использовании пламенно-ионизационного детектора достигает 10 8 г в пробе. [36]
Бесцветный комплекс ртути ( П) отличается от комплексов цинка и кадмия большей реакционной инертностью. Скорость образования комплекса не отличается от скорости образования остальных двухзарядных ионов, если наполнение происходит из раствора Hg ( NO3) 2, не содержащего буферной смеси. [37]
Исследование состава комплекса цинка с К.О. Для исследования состава комплекса цинка с КО применяют различные методы. Сначала приготавливают и анализируют изомолярную серию растворов. [38]
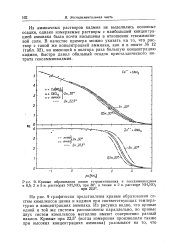 |
Кривые образования ионов тетрамминцинка и гексамминкадмия в 0 5. 2 и 5 н. растворах NH4NO3 при 30, а также в 2 н. растворе NH4NO3. [39] |
На рис. 9 графически представлены кривые образования систем комплексов цинка и кадмия при соответствующих температурах и концентрациях аммиака. Из рисунка видно, что кривые одной и той же системы расположены параллельно, но кривые двух систем комплексов металлов имеют совершенно разный наклон. [40]
 |
Устойчивость комплексов MR и ковалентная характеристика. [41] |
Из данных табл. 13.5 следует, что устойчивость комплексов цинка, кадмия и ртути с хлорид -, иодид-ионами и ЭДТА, а также комплексов галлия и индия с ЭДТА хорошо согласуется с величиной ковалентной характеристики. Несмотря на увеличение радиусов катионов устойчивость комплексов возрастает. Это показывает, что степень ковалентности связи имеет большее значение, чем размеры ионов. Однако устойчивость гидроксокомплексов не подчиняется уже сформулированному правилу. [42]
На рис. 9 графически представлены кривые образования систем комплексов цинка и кадмия при соответствующих температурах и концентрациях аммиака. Из рисунка видно, что кривые одной и той же системы расположены параллельно, но кривые двух систем комплексов металлов имеют совершенно разный наклон. [43]
На рис. 7 показана кривая функциональной зависимости величины рА комплекса цинка с ЭДТА от рН раствора. КрИЕая показывает, что комплекс наиболее устойчив при рН от 6 до 10 и разрушается как в сильнокислых, так и в сильнощелочных растворах. Для сравнения на той же диаграмме приведена аналогичная кривая для комплекса кальция с ЭДТА, более детально показанная на рис. б ( стр. [44]
Мацуда и Аябе [41] применили приведенную теорию для исследования гидроксильных комплексов цинка. [45]
Страницы: 1 2 3 4