Тетраэдрический комплекс
Cтраница 1
Тетраэдрические комплексы не образуют геометрических изомеров. Однако они являются потенциально оптически активными, как и тетраэдрический атом углерода. Наиболее простой вид оптической изомерии, проявляемой большинством органических соединений с четырьмя различными заместителями при атоме углерода, в химии комплексных соединений наблюдается редко. Обычно заместители в тетраэдрических комплексах слишком лабильны, поэтому трудно выделить отдельный комплекс с четырьмя различными лигандами; такие комплексы быстро рацемизируются. [1]
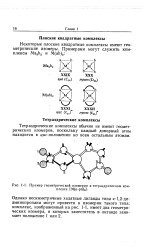 |
Пример геометрической изомерии в тетраэдрическом комплексе [ М ( к-рп 2 ]. [2] |
Тетраэдрические комплексы обычно не имеют геометрических изомеров, поскольку каждый донорный атом находится в г с-положении ко всем остальным атомам. [3]
Тетраэдрические комплексы Ni ( II) типа [ Ni ( PhsAsO) 2Br2 ] и Nil2 ( PPh) z не характерны. Зеленая или красная окраска некоторых из этих комплексов определяется полосой переноса заряда, которая тянется из ультрафиолетовой в видимую область. [4]
Тетраэдрические комплексы Ni ( II), по-видимому, не должны столь легко образовываться, поскольку потеря ЭСКП велика. Основное условие при таком синтезе заключается в том, чтобы использовать большие лигапды, для которых координационная емкость шесть невозможна и которые создают относительно слабое кристаллическое поле. [5]
Тетраэдрические комплексы никеля немногочисленны. Для Ni ( II) очень характерны хелатные комплексы, в том числе с ЭДТА. Ниже приведены основные классы соединений элементов семейства железа и некоторые их важнейшие представители. [6]
Тетраэдрические комплексы переходных металлов характеризуются несколькими новыми чертами, обусловленными наличием ( J-оболочки. [7]
Плоские и тетраэдрические комплексы реагируют по механизму SN2, ассоциативному. [8]
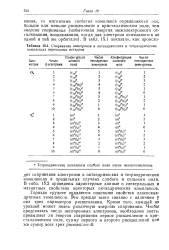 |
Спаривание электронов в октаэдрических и тетраэдрических комплексах переходных металлов. [9] |
Тетраэдрические комплексы слабого поля очень немногочисленны. [10]
Тетраэдрические комплексы ионов переходных металлов обычно устойчивы только при некоторых определенных условиях. Особое исключение представляют ионы [ FeCl4 ] 2 -, [ CoX4 ] 2 - ( X C1, Br, I, NCS) и некоторые ионы [ СоХ3 ( Н2О) ] -; эти частицы сохраняют в водном растворе тетраздрическую геометрию, хотя можно было бы ожидать их акватации с образованием октаэдричеоких ионов. Ни один из них не сохраняет этой геометрии в координирующихся растворителях, таких, как вода или спирты. Большинство тетраэдрических комплексов - анионы или нейтральные молекулы, [ МХ4 ] 2 -, [ MLX3 ] - или [ ML2X2 ], где М - Со, Ni или Fe, L - нейтральный лиганд ( Н2О, пиридин, POR3, AsOR3, PR3, AsR3, NR3), a X - анион, обычно галогенид. [11]
Поэтому тетраэдрические комплексы обычно менее устойчивы, чем октаэдрические, особенно когда последние являются спин-спаренными [ A / / L максимальна; уравнение (7.1), табл. 7.4 ], если другие факторы, такие, как поляризуемость ли-ганда или стерические факторы, не приводят к образованию тетраэдрической конфигурации. Отсюда также следует, что тетраэдрические спин-спаренные комплексы должны реже встречаться, чем октаэдрические спин-спаренные комплексы, и до сих пор образование их не было подтверждено. [12]
Поэтому тетраэдрические комплексы типа [ МАгВ2 ] ( где М - центральный атом, а А и В - лиган-ды) не имеют изомеров. Другое наблюдается в комплексах платины ( II); например, [ РЦЫНзЬСЬ ] встречается в двух изомерных формах, отличающихся по цвету, растворимости, дипольному моменту, реакционной способности и способам получения. [13]
 |
Пространственное строение изомера. [14] |
Поэтому тетраэдрические комплексы типа [ МА2В2 ] ( где М - центральный атом, а А и В - ли-ганды) не имеют изомеров. Другое наблюдается в комплексах платины ( II); например, [ Р МНзЬСЬ ] встречается в двух изомерных формах, отличающихся по цвету, растворимости, дипольному моменту, реакционной способности и способам получения. [15]
Страницы: 1 2 3 4