Переходный комплекс
Cтраница 1
Переходный комплекс может появиться и без предварительного акта разряда и образования адсорбированного атома водорода. Для этого необходимо, чтобы один из двух находящихся по соседству адсорбированных ионов водорода приобрел электрон. Электрохимическая десорбция, по Гориучи, не обязательно должна проходить через разряд гидроксониевого иона на поверхности металла, уже частично покрытой атомами водорода. [1]
Переходный комплекс в этом случае будет иным, но частично сохранит характер карбониевого иона, и поэтому ге-метоксизаместитель должен ускорять дегидратацию, хотя, с другой стороны, величина такого ускорения зависит от той неизвестной доли, в которой катионный заряд принят бензильным углеродным атомом. [2]
Переходный комплекс соответствует такому состоянию химической системы, при котором потенциальная энергия на пути реакции достигает относительного максимума. Но если выбрать иной путь, то на нем этот максимум будет еще больше. Поэтому в точках, отвечающих переходному комплексу, потенциальная поверхность имеет седловину, т.е. она опускается вниз к областям исходных и конечных состояний и поднимается вверх слева и справа к точкам, которые не лежат на пути реакции. [3]
Здесь переходный комплекс, вероятно, принадлежит к двухцентровому типу, а действие среды по общему убеждению сводится к влиянию ее диэлектрических свойств. Можно представить себе, что реакции SA2 постепенно переходят в реакции SNl, когда нуклеофильность атакующего реагента уменьшается, энергия активации растет, и молекула галогенпроизводного приобретает необходимую структуру для того, чтобы соответствующий кароониевыи ион стал достаточно устойчивым. Не подлежит сомнению, что в стабилизации иона карбония важную роль играют также диэлектрические свойства растворителя. [4]
Верхнепермско-триасовый переходный комплекс представлен терригенными ( красноцветными и сероцветными), карбонатными и эффузивными породами. [5]
Относительно переходного комплекса предполагалось, что связь R-С в нем разорвана и, следовательно, соответствующая ей силовая константа равна нулю. [6]
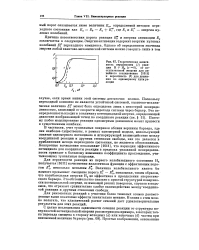 |
Теоретическая зависимость вероятности ( 1 реакции Н Н2 ( v 0, от по ступательной энергии для лилейного столкновения и вероятность ( 2 для движения по одномерному пути реакции. [7] |
Поскольку переходный комплекс не является устойчивой системой, квантово-механи-ческая величина Ef может быть определена лишь с некоторой неопреде - ленностью, зависящей от скорости перехода системы через барьер. Поэтому любое моделирование реакции одномерным движением может привести к существенным ошибкам. [8]
Если переходный комплекс отождествить с обычной молекулой, то движение, о котором идет речь, можно уподобить некоего рода колебательному движению, разрывающему молекулу на части. [9]
Возникает переходный комплекс ( переходное состояние), в котором в результате одновременного присоединения одной группы ( гидроксил) и отщепления другой ( галоген) происходит образование и разрыв ковалентных связей. Причем гидроксильный анион атакует молекулу галогево-алкана со стороны, противоположной галогену, уходящему в виде аниона. Переходное состояние имеет энергию активации большую, чем исходное и конечное состояния системы. [10]
Возникает переходный комплекс ( переходное состояние), в котором в результате одновременного присоединения одной группы ( гидроксил) и отщепления другой ( галоген) происходят образование и разрыв ковалентных связей. Причем гид-роксильный анион атакует молекулу галогеноалкана со стороны противоположной галогену, уходящему в виде аниона. [11]
Этот переходный комплекс затем образует новую Са-связь между Ti и олефином; дальнейший рост цепи происходит путем миграции цепи и присоединения следующего олефина к первоначальному центру связывания. [12]
Если переходный комплекс имеет более высокий ди-польный момент, чем реагенты, то скорость реакции будет возрастать в более полярном растворителе. [13]
Если переходный комплекс имеет более высокий дипольный момент, чем реагенты, то скорость реакции будет возрастать в более полярном растворителе. Если переходный комплекс имеет более низкий общий дипольный момент, чем реагенты, то в более полярном растворителе скорость реакции уменьшится. [14]
Часть переходных комплексов может распасться на исходные продукты. [15]
Страницы: 1 2 3 4