Слабый комплекс
Cтраница 2
Это случай слабых комплексов, сдвиг линий в спектрах ЯМР не зависит от количества адсорбированного вещества. [16]
Константы образования слабых комплексов; комплексы состава 1: 1 ма-лат-иона с катионами щелочных металлов в водном растворе. [17]
В кристаллах слабых комплексов межмолекулярные расстояния определяются ван-дер-ваальсовыми радиусами, тогда как при образовании сильных КПЗ происходит локальная перестройка структуры, сопровождающаяся уменьшением межмолекулярных расстояний. Именно в этих последних случаях, когда возникают условия для сильных межмолекулярных взаимодействий, наиболее ярко проявляются особые магнитные ( сигнал ЭПР) и полупроводниковые свойства КПЗ. [18]
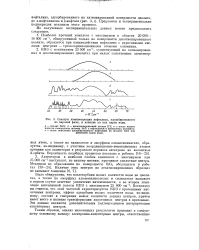 |
Спектры люминесценции нафталина, адсорбированного из паровой фазы, и влияние на них паров воды. [19] |
Акцептором в наиболее слабом комплексе с максимумом при 25 000 см 1 выступают, по нашему мнению, протонные кислотные центры. [20]
Однако если образуются очень слабые комплексы или если В присутствует в следовых концентрациях, то член ( А - а) в уравнении ( 3 - 4) примерно равен нулю, и этот метод нельзя использовать. [21]
В случае образования слабых комплексов ( см. рис. VI.2, в и г) более чувствителен AgBr -, нежели Agl-электрод, и оба комплекса, а также свободный CN -, реагируют с AgBr или Agl. Появляющиеся в результате этого Вг или I и определяют потенциал. [22]
При образовании некоторых слабых комплексов с ароматическими углеводородами наблюдается некоторое возрастание диамагнетизма, свойственного ароматическим молекулам, за счет усиления дело-кализации it - электронов. В других случаях, напротив, образование комплексов сопровождается уменьшением диамагнетизма [69], а в некоторых случаях магнитная восприимчивость комплекса становится положительной. Эго объясняется парамагнетизмом неспаренных элекгрэнэз, пэлвившяхся в комплексе. [23]
Возможное существование таких слабых комплексов может быть обосновано с помощью метода ЛККФ. Наоборот, подход ЛККФ - НМФДМОП переоценивает их устойчивость. Дальнейшее обсуждение дано в гл. [24]
 |
Спектры поглощения. [25] |
Самое низкое возбужденное состояние слабых комплексов должно соответствовать почти полному переводу электрона от донора к акцептору. Именно этот переход электрона от донора к акцептору при поглощении света и является причиной появления в спектре поглощения полос, которых нет в спектрах поглощения молекул, образующих комплекс, и которые называют полосами поглощения переноса заряда. [26]
Рассмотрены методические вопросы исследования слабых комплексов с водородной связью в сжиженных благородных газах. Обсуждены колебательные спектры взаимодействующих молекул ( HHal, CfcNg. [27]
Эфирный атом кислорода способен образовывать слабые комплексы с трех-фтористым бором. При наличии эпоксидных групп при комнатной тем пературе BF3 образует комплексы с эфирным атомом кислорода эпо ксидного цикла, что вызывает отверждение при низких температурах Многоатомные спирты, используемые для образования комплексов с трех-фтористым бором, выполняют двойную функцию. С одной стороны, они способствуют равномерному распределению катализатора в реакционной смеси, с другой - участвуют в реакциях отверждения. [28]
Напротив, с никелем образуется очень слабый комплекс, так как он в присутствии этого комплексо-образующего вещества реагирует с реактивом Чугаева. Только очень большие количества ( более 50 г) N, jST - диоксиэтилглицина препятствуют осаждению никеля. Это обстоятельство было использовано авторами для простого определения никеля в присутствии железа и кобальта. Они поступали следующим образом: к раствору прибавляли приблизительно двукратное по отношению к требуемому для маскирования кобальта и железа количество К, N-диоксиэтилглицина, затем прибавляли реактив Чугаева, нагревали раствор до кипения, слабо подщелачивали аммиаком и через час фильтровали. Полученные ими этим методом результаты вполне удовлетворительны. [29]
Щелочноземельные элементы образуют с ЭДОФГ весьма слабые комплексы, потенциометрическое исследование которых затруднено одновременными реакциями нейтрализации лиганда. При взаимодействии ЭДОФГ с катионами переходных металлов первоначально образуется водородный комплекс MeH2L, в котором фенольные группы не диссоциированы. [30]
Страницы: 1 2 3 4