Слабый комплекс
Cтраница 3
Мп вытесняют ионы магния из сравнительно слабого комплекса его с ЭДТА. [31]
Экспериментальные результаты, относящиеся к слабым комплексам, обнаруживают прямо противоположную картину. IV рассмотрены возможные причины этой аномалии. Эти эффекты, однако, не должны существенно влиять на характеристики ППЗ достаточно прочных комплексов. [32]
Так же как и в сравнительно слабых комплексах галогенов, в значительно более прочных комплексах соединений металлов III группы молекулы доноров не подвергаются существенной перестройке. Что касается положения молекулы донора по отношению к ДА-связи в комплексах Д - МХ3, то оно приблизительно такое же, как и в комплексах с галогенами. [33]
Так как многие неорганические лиганды образуют слабые комплексы, то могут потребоваться высокие концентрации лиганда. В исследованиях такого типа часто используются растворы с концентрациями ЗМ или 4М по ионам натрия или перхлората. Однако не всегда удобно использовать высокую концентрацию солевой среды; при этом важными факторами являются стоимость и время приготовления больших количеств высоко очищенного материала. Кроме того, иногда требуется экстраполировать значения стехиометриче-ских констант, измеренных при нескольких значениях ионной среды к бесконечному разбавлению, чтобы получить значения термодинамических констант устойчивости ( см. гл. В); в таких случаях концентрацию фонового электролита целесообразно поддерживать по возможности более низкой при условии соответствующего контроля коэффициентов активности. [34]
Возможно, что выделение таллия из очень слабого комплекса, образующегося даже в щелочной среде, протекает также обратимо. [35]
Уравнение (5.19) справедливо для растворов не слишком слабых комплексов, содержащих достаточно большой избыток свободного лиганда. Лингейн [3] показал, что восстановление ионов РЬ ( II) на ртутном катоде в щелочной среде протекает в обратимых условиях. [37]
Остальные катионы щелочноземельных металлов вследствие образования более слабых комплексов вытесняют цинк лишь частично и мешают определению кальция. На полярограмме, изображенной на рис. 24, показана зависимость высоты волны кальция от его концентрации. [38]
Этот процесс наиболее вероятен при образовании слабых комплексов донорно-акцепторного типа. Изучение интенсивности такой полосы дает возможность определить состав и оценить константу равновесия комплекса. [39]
Интересно подчеркнуть, что даже в слабых комплексах при незначительных б ( доля перенесенного заряда) и к ( доля ионности основного состояния) вклад в энергию связи энергии взаимодействия с переносом заряда может быть значительным. [40]
Как видно из рис. 56, самые слабые комплексы образует с большей частью катионов ЭДДИФ; самые прочные - ЭДУФ. Прочность комплексов ЭДТФ и ДТПФ почти одинакова и несколько ниже прочности комплексов с ЭДУФ. Следует отметить, что все без исключения кривые ( см. рис. 56) имеют максимум у Си, наиболее четко выраженный в случае ЭДДИФ. Большая часть переходных металлов образует с фосфорсодержащими кислотами менее прочные комплексы, чем с ЭДТА, комплекс же Сц2 с этилендиаминдиизопропилфос-фоновой кислотой по устойчивости превосходит на 2 порядка комплексы Си2 с ЭДТА. [42]
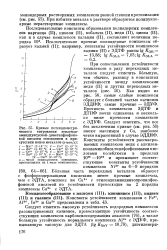 |
Кривые потенциометри-неского титрования этиленди-аминдиуксусной - диметилфосфоно-вой кислоты основанием в присутствии ионов металлов ( г-ион / л. [43] |
Как видно из рис. 56, самые слабые комплексы образует с большей частью катионов ЭДДИФ; самые прочные - ЭДУФ. Прочность комплексов ЭДТФ и ДТПФ почти одинакова и несколько ниже прочности комплексов с ЭДУФ. Следует отметить, что все без исключения кривые ( см. рис. 56) имеют максимум у Си, наиболее четко выраженный в случае ЭДДИФ. [44]
Желательно, чтобы солевая среда могла давать только слабые комплексы с реагентами и не привносила ничего в изучаемые свойства; например, среда должна мало поглощать при длинах волн, используемых при спектрофотометрических исследованиях. К сожалению, влияние компле-ксообразования на некоторые физические свойства раствора ( например, на его электропроводность) может быть в значительной степени смазано в присутствии солевой среды. Важным фактором является растворимость буферного электролита, особенно при исследованиях в органических или смешанных водно-органических растворителях. [45]
Страницы: 1 2 3 4