Перекисный комплекс
Cтраница 2
Метод основан на измерении светопоглощения растворов перекисного комплекса молибдена в сернокислой среде при 368 нм. Необходимо внесение поправки на содержание урана. [16]
Наибольший интерес представляет определение церия в виде перекисного комплекса. Предложены различные варианты метода. [17]
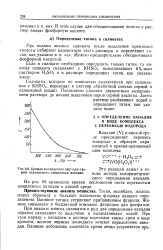 |
Кривая поглощения света раствором перекисного комплекса ванадия. [18] |
На рис. 68 приведена кривая поглощения света перекисным комплексом ванадия в кислой среде. [19]
Чане считает, что идентичность полос Соре в перекисных комплексах с Н2О2 и гидроперекисью метила или этила указывает на то, что замещение в молекуле Н2О2 не влияет на природу связи железо-перекись. Теорелл [20, 51] исходя из магнетохимических исследований предположил, что эта связь во вторичных бледнокрасных комплексах ковалентна, в то время как сравнение спектров первичных зеленых комплексов с зеленым фторид-пероксидазным комплексом, связи в котором, как известно, ионные, показывает, что в этих первичных комплексах связь ионная. [20]
Мешают, в первую очередь, элементы, образующие окрашенные перекисные комплексы, в частности, титан, а также железо и молибден. Титановый комплекс может быть разрушен фторид - ионами, в то время как ванадиевый комплекс устойчив по отношению к последним. Помехи со стороны железа устраняются связыванием его в фосфатный комплекс. [21]
Ниобий ( У) и тантал ( У) образуют прочные растворимые фторидные, тартрат-ные, оксалатные, перекисные комплексы, а также неустойчивые сульфатные комплексы, причем комплексы ниобия прочнее соответствующих соединений тантала. [22]
Исследование влияния Ti V, Fein и фосфат-иона на образование перекисного комплекса ниобия в сернокислых растворах. [23]
В работе [16] предложено одновременное спектрофотомет-рическое определение Nb и Та в виде перекисных комплексов, основанное на том, что максимумы погашения этих комплексов лежат в разных областях ультрафиолетовой части спектра. В статье имеются указания о возможности разработки в аналогичных условиях дифференциального спектрофотометрического метода. [24]
Однако единственной серьезной помехой является титан, который в аналогичных условиях также образует перекисный комплекс. [25]
Ввиду отсутствия прямых доказательств все имеющиеся в настоящее время аргументы относительно природы этих перекисных комплексов могут основываться только на аналогиях с другими производными гемопротеинов и их реакциями. Предположение Чанса о том, что первичные комплексы каталазы испытывают атаку на порфириновое кольцо, не кажется вполне правдоподобным, если произвести сравнение с пероксидазой. Первичный комплекс пероксидазы напоминает первичный комплекс каталазы, особенно в области Соре, однако структура с видоизмененным порфириновым кольцом приписывается комплексу IV, который образуется с пероксидазой в присутствии избытка гидроперекиси алкила. В видимой области спектры первичных комплексов похожи на спектры свободных энзимов; очень большая скорость образования комплексов, а в случае каталазы преимущественное образование их в присутствии цианида - все это наводи на мысль о том, что этот процесс образования включает простое бимолекулярное замещение. Большое сродство гематиновои группы этих энзимов к перекиси водорода свидетельствует о том, что связывание молекулы Н2О2 как таковой исключается, так как этот тип реакции относится к реакциям замещения связанного аниона ОН сольватационной Н2О2, а в отношении этой реакции можно сделать вывод при учете изменений теплоты и энтропии, что она не может быть осуществлена. Интересно отметить, что соединения этого типа не ограничиваются гемо - - протеинами. [26]
Последнее можно объяснить тем, что с иодидом реагирует не только На02, а преимущественно перекисный комплекс катионных форм циркония. Растворы солей циркония в НС1 ( от 1 до 5 М) одинаково катализируют реакцию. С повышением рН каталитическое действие солей циркония резко падает. [27]
Они вступают в действие лишь после того, как кислород уже закрепляется оксидазой в виде перекисных комплексов. Ускоряя окислительное действие этих перекисных комплексов, соли металлов играют здесь роль вторичных катализаторов медленного сгорания, о которых была речь выше. [28]
Основываясь на этих данных, американские авторы [274] измерили относительные скорости окисления циклогексена и норборнена с помощью перекисного комплекса МоО5 - ГМФТА. Поскольку существенной разницы скоростей не обнаружено, то диполярный механизм признан ими маловероятным. [29]
Недавно [ 62, в ] было исследовано влияние некоторых факторов на скорость потери концентрации активного кислорода перекисным комплексом СеШССНзЬССКШа СбН5 ( СНз) гСООН в растворе кумола. Авторы цитированной выше работы считают, что понижение концентрации перекисного кислорода со временем может быть удовлетворительно описано кинетическим уравнением реакции, если учесть степень димеризации исходного перекисного комплекса. С другой стороны следует учесть, что, согласно данным их предыдущей работы [ 62, б ], даже при более низкой концентрации этот комплекс находится практически полностью в димерном состоянии. Такие разноречивые данные одних и тех же авторов едва ли можно объяснить влиянием природы растворителя ( бензол и кумол), а также температуры, изменение которой для результатов обеих работ составляло всего лишь 45 С. По нашему мнению, обработка результатов кинетических наблюдений в работе [ 62, в ] слишком упрощена, что привело се авторов к недостаточно обоснованным выводам. В частности, они совсем не учитывали возможности образования гидроперекиси кумола в результате окисления растворителя ( кумола) кислородом, выделившимся при разложении исходного перекисного комплекса. [30]
Страницы: 1 2 3 4