Перекисный комплекс
Cтраница 3
На всех простых окислах - полупроводниках углеводороды сорбируются с большой скоростью и реагируют с кислородом газовой фазы с образованием перекисного комплекса, который служит промежуточным продуктом. [31]
В областях синтеза новых перекисных соединений, применения методов меченых атомов и физико-химического анализа к изучению их свойств, исследования перекисных комплексов, каталитического разложения растворов перекиси водорода, советские ученые занимают передовые позиции. Однако недостаточно развиваются экспериментальные и теоретические работы по химической термодинамике перекисных соединений и процессов, протекающих с их участием. Имеется значительное отставание в области аналитической химии перекисных соединений и в рентгеноструктурных исследованиях. Область реакционной способности неорганических перекисных соединений глубоко не затронута ни советскими ни зарубежными учеными. Слабо развиваются исследования по кинетике. [32]
Выше рН 8 8, когда дальнейшее уменьшение концентрации водородных ионов ведет к увеличению степени образования щелочной перо-ксидазы, образование перекисного комплекса замедляется, свидетельствуя о том, что перекиси не могут замещать ковалентно связанную гидроксильную группу. [33]
Перекисные комплексы, не являющиеся дероксокислотами или производными пероксокислот, в большинстве случаев гидролизуются с образованием перекиси водорода, но некоторые многоядерные перекисные комплексы, как, например, [ ( NH3) 5Co - О-О - Go ( NH3) 5 ] 5, весьма устойчивы к воде. [34]
Скорость реакции в данном случае не зависит от концентрации перекиси водорода; последнее можно объяснить тем, что с яодидом реагирует преимущественно перекисный комплекс ка - ионных форм циркония. [35]
Скорость реакции в данном случае не зависит от концентрации перекиси водорода; последнее можно объяснить тем, что с яодидом реагирует преимущественно перекисный комплекс ка-гионных форм циркония. [36]
Каталитическое действие многозарядных ионов в электрохимическом восстановлении перекиси водорода во многом аналогично их действию в обычных окислительно-восстановительных реакциях и обусловлено образованием перекисных комплексов. [37]
Если растворы циркония и гафния или осадки их гидроокисей, а также фосфатов обработать перекисью водорода и едким натром, в растворе образуются перекисные комплексы. При нагревании щелочных растворов перекисные комплексы циркония и гафния разрушаются и в осадок выпадают гидроокиси. Хевеши [47] утверждает обратное, что при нагревании перцирконат разлагается в первую очередь и осадки обедняются гафнием. [38]
Скорость реакции в данном случае не зависит от концентрации перекиси водорода; последнее можно объяснить тем, что с 1 - - ионом реагирует преимущественно перекисный комплекс катионных форм циркония. [39]
Метод основан на том, что ион фтора вступает в реакцию с окрашенным перекисным соединением титана, причем образующийся фторидный комплекс титана диссоциирует слабее, чем перекисный комплекс. В разбавленных растворах реакция идет с образованием монофторидного комплекса титана. [40]
Из приведенного выше механизма реакции непосредственно не следует, что при ингибировании процесса разложения перекиси водорода цианидом не происходит конкурирующих реакций, так как если цианид может участвовать в одной из конкурирующих реакций при образовании перекисного комплекса с выделением кислорода в стадии ( IV), то можно было бы ожидать и протекания конкурирующих реакций при ингибировании. Анализ этой системы в указанных условиях обнаруживает, что здесь при ингибировании конкурирующие реакции не протекают. [41]
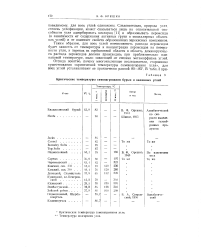 |
Критические температуры самонагревания бурых и каменных углей. [42] |
Следовательно, природа угля, степень углефикации, может сказываться лишь на относительной способности угля адсорбировать кислород [11] и образовывать пероксиды ( в зависимости от содержания активных групп в мицеллярных оболочках углей) и не изменяет свойств образованных перекисных комплексов. [43]
Комплексы кобальта, по-видимому, также содержат перекисную группу, но в данном случае она является мос-тиковой между атомами металла, и хотя точное строение этой группировки неизвестно, вероятно, она построена по типу 13.V6. При подкислении раствора иридиевого комплекса образуется Н2О2, и в основном свойства его аналогичны свойствам других хорошо известных перекисных комплексов ( см. разд. [44]
Цирконий образует прочные комплексы с фторидами, комплек-соном III, оксикислотами. Перекисный комплекс растворяется только в сильно щелочной среде. [45]
Страницы: 1 2 3 4