Перекисный комплекс
Cтраница 4
Существуют растворимые перекисные комплексы циркония в кислой среде с отношением Zr: Н2О2 1: 1 и 1: 2, представляющие продукты присоединения молекул Н2О2 к ионам циркония. [46]
Если растворы циркония и гафния или осадки их гидроокисей, а также фосфатов обработать перекисью водорода и едким натром, в растворе образуются перекисные комплексы. При нагревании щелочных растворов перекисные комплексы циркония и гафния разрушаются и в осадок выпадают гидроокиси. Хевеши [47] утверждает обратное, что при нагревании перцирконат разлагается в первую очередь и осадки обедняются гафнием. [47]
Они вступают в действие лишь после того, как кислород уже закрепляется оксидазой в виде перекисных комплексов. Ускоряя окислительное действие этих перекисных комплексов, соли металлов играют здесь роль вторичных катализаторов медленного сгорания, о которых была речь выше. [48]
Из этих металлов наибольшее влияние оказывает ванадий. При 410 нм поглощение перекисного комплекса ванадия составляет примерно четверть поглощения соответствующего комплекса титана. [49]
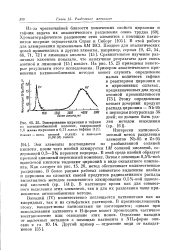 |
Элюирование циркония и гафния лен методом осаждения. [50] |
Эти элементы поглощаются из разбавленной соляной кислоты, после чего ниобий элюируется 1М соляной кислотой, содержащей 0 3 - 3 % перекиси водорода. В этой среде ниобий образует прочный анионный перекисный комплекс. Затем с помощью 0 5 % - ной щавелевой кислоты выделяют цирконий в виде оксалатного комплекса. [51]
Первый период - самонагревание угля до темпег ратуры 76 - 85 С ( критическая температура самонагревания угля), при которой поглощение кислорода сопровождается образованием низкотемпературных перекис-ных комплексов ( СО2, Н Э), вследствие чего вес угля несколько увеличивается. Второй период - интенсивное самонагревание угля выше температуры 85 С, при которой низкотемпературные перекисные комплексы неустойчивы и процесс их распада сопровождается еще-большим выделением тепла с испарением влаги. Вяеш-ним признаком наличия в штабеле этой температуры служат влажные пятна на его поверхности. Третий период ( при температуре выше il30 - J170 С) - образование высокотемпературных комплексов, когда скорость выделения тепла становится весьма значительной и температура быстро растет, приближаясь к температуре возгорания угля. Четвертый период - достижение температуры возгорания, когда процесс переходит в фазу горения, сопровождающуюся дымообразоваяием и озо-лением топлива. [52]
При реакции с перекисью наблюдается такой же индукционный период, как и при реакции оксалата. Однако индуцированное окисление соляной кислоты не имеет места, что связано, по-видимому, с образованием перекисного комплекса Мпш, стабилизирующего состояние кислоты. [53]
Вследствие того что на поверхности платины находятся атомы со свободными валентностями, в первую очередь происходит активированная адсорбция кислорода, обусловленная возникновением электронной связи. В результате химического взаимодействия кислорода с поверхностью платины ослабляются связи между атомами в молекулах О2 и образуется перекисный комплекс катализатор - кислород. [54]
Недавние опыты Кейлина и Хартри [ 45, с полной очевидностью показавшие, что метгемоглобин и метмиоглобин восстанавливаются, когда они реагируют с перекисью водорода в концентрации, достаточной для каталитического разложения, а также их прежние результаты [16, 17], свидетельствующие о восстановлении азид-каталазы перекисью водорода, являются бесспорным доказательством того, что для разложения перекиси с помощью гемопротеинов возможен такой путь реакции, который включает изменение валентности. Трудно, однако, предложить какой-либо механизм для реакций метгемогло-бина и метмиоглобина, потому что и здесь участвует перекисный комплекс не определенной структуры. [55]
Страницы: 1 2 3 4