Водородный комплекс
Cтраница 1
Водородный комплекс является промежуточным продуктом, и прочность его незначительна. Константа диссоциации протониро-ванных комплексов двухвалентных катионов равна приблизительно 10 - 3, у трехвалентных эта величина несколько больше. Прочность же нормальных комплексов, как и следовало ожидать, высокая. [1]
Водородные комплексы Си, Cd, Ni и Zn малорастворимы в воде, на чем и основано их выделение. Так, в области рН 3 - 6 выделяются этилендиаминбисметилфосфонаты свинца, в области рН 2 5 - 4 эти-лендиаминтетраметилфосфонаты редкоземельных элементов. [2]
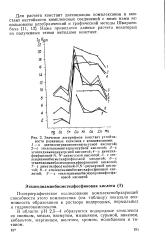
При титровании водородного комплекса HCrY Н20 щелочью комплекс сохраняет до наступления первой точки эквивалентности свою фиолетовую окраску и его кривая экстинкции не меняется. Очевидно, происходит отщепление иона водорода из свободной карбоксильной группы, что не меняет координационной сферы иона металла, играющей роль в поглощении света. [3]
При этом прочность водородных комплексов выше таковой соответствующих комплексов карбоксилсодержащих аналогов. [4]
Значительная величина констант устойчивости водородных комплексов изучаемых соединений по сравнению с таковыми для карбоксилсодержащих аналогов, вероятно, может быть объяснена увеличенной дентатностью фосфиновой группы по сравнению с ацетатной. Увеличенная дентатность в этом случае является следствием того, что в одной фосфиновой группе два кислородных атома связываются с атомом металла. [5]
В энергетике водород может найти применение в ядерно-технологических водородных комплексах, на пиковых электростанциях, для аккумулирования энергии возобновляемых источников, в автомобильной и авиационной промышленное-тях - как добавка к традиционному топливу или как топливо, в металлургии - для получения металлов методом прямого восстановления руд. [6]
В области рН 2 5 - 4 образуются водородные комплексы со свинцом, медью, висмутом, мышьяком, сурьмой, никелем, кобальтом, марганцем, железом, хромом, молибденом и титаном. [8]
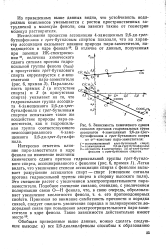 |
Зависимость химического сдвига сигналов протонов гидроксидьных групп ассоциатов 4-замещенных 2 6-ди-грег - бутилфенолов и трег-бутилового спирта. [9] |
Из приведенных выше данных видно, что устойчивость водородных комплексов уменьшается с ростом цространственных затруднений в молекуле фенола; она зависит также от геометрии молекул растворителя. [10]
Сделанный нами вывод относительно способности фосфорилированных комплексов к образованию прочных водородных комплексов, основанный на использовании при взаимодействии с катионами только донорных функций кислородов фосфоновых групп, явился основанием для целенаправленного синтеза серии комплексообразующих реагентов, содержащих две фосфоновые группы у одного углеродного атома. [12]
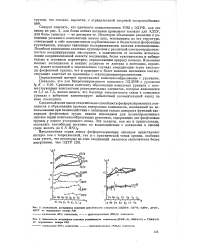
Потенциометрическое исследование подтвердило полярографические данные и позволило доказать, что образование водородных комплексов происходит при наличии бетаиновых водородов в комплексоне. На рис. 3 представлены некоторые из полученных данных. [13]
Дополнительная энергия ( и энтропийный эффект) активированного комплекса складывается из соответствующих значений водородных комплексов, электроно-донорно-акцепторных или комплексов с переносом заряда и комплексов долгоживущих свободных стабильных радикалов. [14]
ЭДТА образует с кальцием нормальные комплексы CaY2 - Og caY 10 96), водородные комплексы CaHY, гидроксокомплек-сы CaY ( OH) 3 и смешанные комплексы типа CaYX -, где X - одновалентный лигаид. Образование высших комплексов не наблюдается. [15]
Страницы: 1 2 3