Водородный комплекс
Cтраница 3
В большинстве случаев комплексы ЭДТА хорошо растворимы в воде и практически нерастворимы в спирте, что и используется для выделения их в твердом виде. При этом в зависимости от условий синтеза могут быть выделены комплексные кислоты типа H MeY ( водородные комплексы) и нормальные комплексы типа Ме, [ MeY ], где Me и Me могут быть одним и тем же или разными катионами. [31]
Если известна величина константы Крепц, то можно при помощи потенциометрического метода с платиновым электродом определить и константу КРешх. Однако эта система значительно сложнее, чем кажется, так как наряду с участием в равновесии гидроксокомплексов и водородных комплексов следует также предположить участие и смешанного ацетатнитрилтриуксусного комплекса с ионами трехвалентного железа ( XIX), поскольку измерения Шварценбаха и Геллера проводились в ацетатном буфере. [32]
Значения констант KMHY очень малы. У комплексов двухвалентных катионов они равны приблизительно 103, у трехвалентных - 102 и меньше, та к что при проведении опытов в растворах с рН выше 4 поправка на образование водородного комплекса практически всегда лежит в пределах ошибок опыта. [33]
В большинстве случаев комплексы ЭДТА хорошо растворимы в воде и практически нерастворимы в спирте, что и используется для выделения их в твердом виде. При этом в зависимости от условий синтеза могут быть выделены комплексные кислоты типа H. MeY ( водородные комплексы) и нормальные комплексы типа Ме, [ MeY ], где Me и Me могут быть одним и тем же или разными катионами. [34]
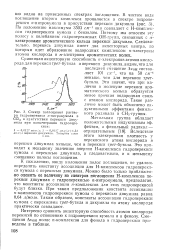 |
Спектр поглощения раствора гидроперекиси л-нитрокумола в СС14 в присутствии перекиси дикумила при концентрации гидроперекиси. [35] |
По положению максимума 3503 см-1 она совпадает с Н - комплек-сом гидроперекиси кумола с бензолом. Поэтому мы относим эту полосу к колебаниям гидроперекисных ОН-групп, связанных с л-электронами ароматического кольца перекиси дикумила. Следовательно, перекись дикумила имеет два акцепторных центра, по которым идет образование водородных комплексов: - электроны атомов кислорода и я-электроны ароматических колец. [36]
Страницы: 1 2 3