Этилендиаминовый комплекс
Cтраница 1
 |
Кремнекислородныи радикал [ Sie016 ] 6 -. [1] |
Этилендиаминовый комплекс в этой структуре имеет гош - гош - гош-конфигурацию. Использование эффекта аномального рассеяния рентгеновских лучей позволило определить абсолютную конфигурацию структуры, показавшую, что этот комплекс имеет форму левого винта. [2]
Отмеченная большая устойчивость этилендиаминовых комплексов по сравнению с аммиачными - явление общее в химии комплексных соединений. Эта закономерность, подчеркивающая стабиливирующее действие циклических заместителей типа этилендиамина, характерна не только для соединений кобальта, но отчетливо обнаруживается и на соединениях других, металлов. [3]
Отмеченная большая устойчивость этилендиаминовых комплексов по сравнению с аммиачными - явление общее в химии комплексных соединений. Эта закономерность, подчеркивающая стабилизирующее действие циклических заместителей типа этилендиамина, характерна не только для соединений кобальта, но отчетливо обнаруживается и на соединениях других металлов. [4]
Электролиты на основе этилендиаминовых комплексов кадмия подробно изучены в Казанском химико-технологическом институте им. В определенных условиях они дают светлые мелкокристаллические плотные осадки кадмия и могут заменять цианистые электролиты. [5]
Для исследованных систем аммиачных и этилендиаминовых комплексов в табл. 9 сравниваются первая константа устойчивости k и общая константа системы комплексов KN с радиусом ионов металлов и первой константой кислотной диссоциации ак-во-ионов металлов. [6]
Кривые образования для систем этилендиаминовых комплексов были лишь частично получены прежде применяемым методом измерения в заранее приготовленных растворах со стеклянным электродом. [7]
Что касается исследованных систем этилендиаминовых комплексов, то нужно отметить, что при расчете статистического эффекта учитывали, что молекула этилендиамина занимает два соседних координационных места, и, таким образом, две молекулы этилендиамина, присоединившиеся первыми, вполне могут занять четыре места в одной плоскости ( см. стр. [8]
Кривые образования для систем этилендиаминовых комплексов были лишь частично получены прежде применяемым методом измерения в заранее приготовленных растворах со стеклянным электродом. [9]
Что касается исследованных систем этилендиаминовых комплексов, то нужно отметить, что при расчете статистического эффекта учитывали, что молекула этилендиамина занимает два соседних координационных места, и, таким образом, две молекулы этилендиамина, присоединившиеся первыми, вполне могут занять четыре места в одной плоскости ( см. стр. [10]
В экспериментальной части приведены результаты исследования аммиачных и этилендиаминовых комплексов металлов. Наличие полной библиографии делает книгу ценным справочником по амминам металлов. [11]
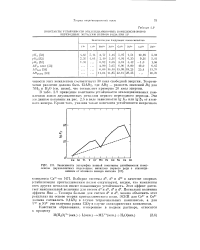 |
Зависимость логарифма полной копстанты устойчивости комплексов двухвалентных переходных металлов первого ряда с этиленди-амином от атомного номера металла. [12] |
В табл. 2.9 приведены константы устойчивости этилендиаминовых комплексов ионов двухвалентных металлов первого переходного периода. Эти же данные показаны на рис. 2.5 в виде зависимости lg KT или lg ( 33 т атомного номера. [13]
При добавлении кобальтинитрита натрия к солянокислому раствору этилендиаминового комплекса образуется кобальтинитрит [ ReO ( OH) ( NH2CH2CH2NH2) 2 ] Co ( N02) 6, а с иодис. Все эти соли лишь слегка растворимы в воде. [14]
Как видно из этих данных, устойчивость этилендиаминовых комплексов весьма высока и по ряду Fe2 - Co2t - Ni2 возрастает. Подобные же по составу комплексы [ NiEn2 ( N03h ] и [ NiEn2NO3 ] ClO4 интересны тем, что в первом из них группа ЫОз занимает одно координационное место, а во втором - два. [15]
Страницы: 1 2 3 4