Тиосульфатный комплекс
Cтраница 1
Тиосульфатные комплексы характерны лишь для двухвалентной платины. Основным их представителем является желтый Na6 [ Pt ( S20s) 4 ] 10H2O, исходя из которого обменным разложением могут быть получены соли ряда других металлов. [1]
Тиосульфатные комплексы характерны лишь для двухвалентной платины. Основным их представителем является желтый Nae [ Pt ( SjO3) 4 ] ЮНгО, исходя из которого обменным разложением могут быть получены соли ряда других металлов. [2]
 |
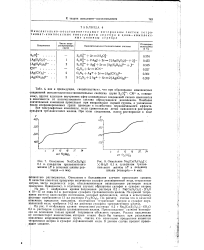
Окисление Nas [ Cu ( S2O3 2 6Н2О н. иодом. [3] |
Все тиосульфатные комплексы меди, хорошо растворимые в воде, в разбавленных растворах количественно окисляются спиртовым раствором иода, а также раствором иода в йодистом калии. При этом в конечном счете получаются осадки Cu2J2 и тетратионат натрия, остающийся в растворе. Этот вывод следует из результатов изучения кривых титрования различных тиосульфатных комплексов меди растворами иода, а также из результатов анализа осадков, образующихся при окислении. [4]
Все тиосульфатные комплексы меди сравнительно легко окисляются раствором сульфата трехвалентного железа. [6]
Кроме аммиачных и тиосульфатных комплексов для серебра характерно образование цианидного комплекса [ Ag ( CN) 2 ] -, который широко используется в качестве электролита при гальваническом серебрении различных изделий. [7]
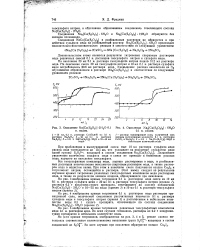
Рассмотрение кривых титрования различных тиосульфатных комплексов меди Приводит к выводу, что соединения, возникающие в смесях разбавленных растворов сульфата меди и тиосульфата натрия, ведут себя при окислении иодом иначе, чем соединения того же количественного состава, но выделенные из смесей насыщенных ( растворов сульфатов меди и тиосульфата натрия. На кривых титрования соединений, юзникающих в разбавленных смесях реагентов, имеется всегда один скачок потенци - 1ла, отвечающий окислению всех групп S8O3 -, входящих в состав комплексов. На f ривых титрования некоторых соединений, выделенных из смесей насыщенных растворов, имеется 2 скачка потенциала, указывающие на раздельное окисление групп Og - На кривой титрования Na3 [ Cu ( S2O3) 2 ] 6Н2О ( рис. 4, кривая 2) имеется скачка потенциала. Второй скачок потенциала резкий и соответствует окислению торой группы. [8]
Очень устойчив также и тиосульфатный комплекс. Этот метод дает хорошие результаты при анализе препаратов, свободных от других соединений ртути. [9]
Таким же способом разрушают цианидные и тиосульфатные комплексы и нерастворимые галогениды серебра. [10]
Следовательно, константа диссоциации тиосульфатного комплекса равна 2 5 - 10 - 33: 6 - 10 - 44 2 - 10 - 30, а для процесса Аи - е 252О2 - Аи ( 52Оз), Е 0 0 1422 В. Поскольку потенциал рассчитан по экспериментальным данным, он не зависит от значения стандартного потенциала золота. [11]
Из кривых потенциометрического титрования тиосульфатных комплексов меди иодом найдены потенциалы соответствующих окислительно-восстановительных систем. [12]
Образующиеся при добавлении тиосульфата к раствору солей свинца тиосульфатные комплексы хорошо экстрагируются данным методом, особенно из нейтральной среды. [13]
Метод применим также для изучения равновесий в растворах тиосульфатных комплексов. [14]
При сравнении потенциалов, при которых происходит окисление тиосульфатных комплексов иодом, обнаруживается, что окислительно-восстановительные свойства тиосульфата изменяются при образовании комплексных соединений в зависимости от количественного состава этих соединений. [15]
Страницы: 1 2 3 4