Тиосульфатный комплекс
Cтраница 2
Из комплексных соединений рения с неорганическими лигандами известны также сульфатные, сульфитные и тиосульфатные комплексы, которые, однако, не выделены в твердом состоянии. В то же время они используются для спектрофотометрического определения рения и поэтому описаны в гл. Многочисленные комплексные соединения рения с органическими лигандами, используемые в анализе, рассмотрены в соответствующих главах. [16]
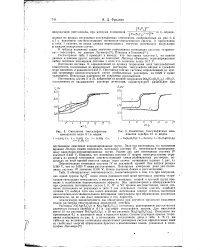 |
Окисление тиосульфатных комплексов меди н. иодом.| Окисление тиосульфатных комплексов серебра н. иодом. [17] |
Потенциал системы II, определенный из кривых титрования всех тиосульфатных комплексов, выделенных из насыщенных растворов тиосульфата натрия и сульфата меди одинаков и равняется 0.455 V. Потенциал той же системы, определенный из кривой титрования соответствующей смеси разбавленных растворов, на 0.029 V выше указанного. [18]
Таберн и Шелберг [1447] использовали Н202 для определения золота в тиосульфатном комплексе, а Мюллер [,1260] - для анализа электролитических ванн. В последнем случае комплексные цианиды и органические вещества вначале разрушают нагреванием с 2-кратным избытком смеси НСЮ4 - ( - HN03 ( 1: 1), а затем восстанавливают золото перекисью водорода. [19]
Установлено, что в определенных условиях координированные группы, входящие в состав тиосульфатных комплексов меди, могут окисляться иодом раздельно. Аналогичные результаты были получены при изучении кривых титрования иодом растворов тиосульфатных комплексов серебра. [20]
При пользовании этими формулами возможна следующая интерпретация полученных нами экспериментальных результатов при окислении тиосульфатных комплексов меди иодом. Можно предполагать, что циклический ион более устойчив, чем ион, имеющий линейное строение. Соответственно, ион [ Cu ( S2O3) ] - должен окисляться при более высоких потенциалах, чем ион [ Cu ( S8O3) 2 ] 3 -, что соответствует действительности. [21]
В литературе описан метод разделения меди, кадмия и цинка, основанный на различной устойчивости тиосульфатных комплексов. [22]
В качестве же примера комплексных ионов с весьма высокой степенью ковалентности можно привести комплексные иодиды, тиосульфатные комплексы, центральными ионами в которых являются ноны с 18-электронной оболочкой или с незавершенными оболочками. [23]
Другие комплексные ионы серебра, такие, как цианидный комплекс Ag ( CN) - и тиосульфатный комплекс Ag ( S203) T уже были описаны в гл. [24]
Другие комплексные ионы серебра, такие, как цианидный комплекс Ag ( CN) - и тиосульфатный комплекс Ag ( S203) - уже упоминались в гл. [25]
Экспериментально изучено восстановление сульфата двухвалент - ной меди тиосульфатом натрия в насыщенных и разбавленных растворах, а также окислительно-восстановительные свойства ряда возникающих при этом тиосульфатных комплексов меди. [26]
В предыдущем разделе был рассмотрен пример, в котором 82Оз - - ион конкурировал с Вг - - ионом при образовании комплексов с серебром, однако в этом случае мы пренебрегли бромидными комплексами серебра по сравнению с его тиосульфатными комплексами. В этом и следующем разделах будет рассмотрено ком-плексообразование в щелочном растворе, где ОН - ион конкурирует почти на равных условиях с такими лигандами как галоген-и циан-ионы или аммиак. [27]
Интересно отметить, что методом растирания можно осуще ствить и ряд других реакций, не идущих в присутствии воды - Например, открыть Со можно также путем растирания исследуемой смеси с Na2S2O3, причем также наблюдается посинение вследствие образования тиосульфатного комплекса кобальта. [28]
Висмут, кадмий, медь, свинец, ртуть, никель, кобальт, серебро, золото, олово ( II), если присутствуют в не слишком больших количествах ( меньше 5 мг / л), при этом рН связываются в тиосульфатные комплексы и не мешают определению цинка. Лишь тогда, когда отношение концентраций мешающий элемент: цинк превышает 5: 0 05, приходится вводить в анализируемый раствор еще небольшое количество цианида калия. [29]
Висмут, кадмий, медь, свинец, ртуть, никель, кобальт, серебро, золото, олово ( II), если присутствуют в не слишком больших количествах ( меньше 5 мг / л), при этом значении рН связываются в тиосульфатные комплексы и не мешают определению цинка. Лишь тогда, когда отношение концентраций мешающий элемент: цинк превышает 5: 0 05, приходится вводить в анализируемый раствор еще небольшое количество цианида калия. [30]
Страницы: 1 2 3 4