Тиосульфатный комплекс
Cтраница 3
Все вышеприведенные комплексы разлагаются сильными кислотами с возможным выделением наиболее трудно растворимой соли соответственной кислоты. Тиосульфатный комплекс распадается даже при кипячении, причем выделяется осадок черного сернистого серебра. [31]
Все вышеприведенные комплексы разлагаются сильными кислотами с возможным выделением наиболее трудно растворимой соли соответственной кислоты. Тиосульфатный комплекс распадается даже при кипячении, причем выделяется осадок черного сернистого серебра. [32]
Денни и Монк [23] провели более строгое исследование растворимости тиосульфата бария в ряде растворов, содержащих различные катионы. Были рассчитаны устойчивости соответствующих тиосульфатных комплексов и сделано допущение о присутствии ряда форм, находящихся в ступенчатом равновесии. Так как ионная сила не контролировалась, были введены поправки на изменение коэффициентов активности. Например, для йодноватой кислоты было рассчитано значение р 1 по растворимости иодатов серебра [62] и бария [72] в растворах с различной кислотностью, а также получены константы образования ионов кислых сульфатов [42] и кислых селенидов [88] с помощью сульфата серебра и селенида натрия соответственно. [33]
Формулы отдельных соединений были установлены на основании результатов анализов выделенных препаратов с учетом результатов потенциометрических исследований, а равно имея в виду указания Рябчикова и Сильниченко о возможности размещения атомов меди во внутренней и внешней сфере комплекса. Следует отметить, что строение тиосульфатных комплексов меди мало изучено, и мы не имеем безусловных доказательств правильности выбора формул строения некоторых отдельных соединений. [34]
Поскольку здесь серебро уже находилось в виде тиосульфатного комплекса, извлечению серебра из цианидов уделялось мало внимания, за исключением немногих опытов по извлечению серебра из отходов ванн гальванического серебрения, в которых содержались цианиды. [35]
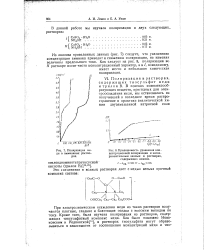 |
Поляризация меди в аммиачных растворах.| Приложимость уравнения концентрационной поляризации к экспериментальным данным в растворах. [36] |
При электролитическом осаждении меди из таких растворов получаются плотные, гладкие и блестящие осадки с высоким выходом по току. Кроме того, была изучена поляризация из растворов, содержащих тиосульфатный комплекс меди. [37]
Известны ацидиметрические приемы определения. Так, при взаимодействии осадков карбоната или гидроокиси серебра с тиосульфатом натрия образуются растворимые тиосульфатные комплексы. [38]
Золото не реагирует с углеродом даже при высоких температурах. Соединение золотэ с этим элементом может быть получено косвенным путем - воздействием ацетилена на раствор тиосульфатного комплекса золота, при этом образуется желтый карбид Аи2С2, точнее ацетилид золота, который крайне взрывоопасен. [39]
Интересно отметить, что методом растирания можно осуществить и ряд других реакций, не идущих в присутствии воды. Например, обнаружить Со2 можно путем растирания исследуемой смеси с Na2S2O3, причем также наблюдается посинение вследствие образования тиосульфатного комплекса кобальта. [40]
Интересно отметить, что методом растирания можно осуществить и ряд ругих реакций, не идущих в присутствии воды. Например, открыть Со11 можно также путем растирания исследуемой смеси с Na2S2O3, причем также наблюдается посинение вследствие образования тиосульфатного комплекса кобальта. [41]
Плутоний переводят в трехвалентную форму обработкой сильнокислого раствора плутония в НС1 5 % - ным раствором SnClj при нагревании. Охлаждают и добавляют равный объем 5 % - ного раствора KCNS, оставляют стоять 2 часа, после чего вольфрам экстрагируют в виде тиосульфатного комплекса двумя порциями эфира ( 3 и 2 мл), предварительно обработанного смесью растворов SnCl2 и KCNS. Органические фазы колориметрируют в колориметре Дюбоска с синим светофильтром, используя стандартную шкалу. Метод позволяет определять 0 005 - 0 1 % вольфрама с точностью 5 отн. Железо и уран не мешают при равных и меньших количествах. В присутствии молибдена получают завышенные результаты. [42]
В водном растворе сера может существовать в виде следующих бесцветных ионов: HS - ( или S2 - при рН11), - HSOjH SO -, SsOg -, HSOI ( при pH2), SO42 -, SaOJ -, S2Of -; оиа может находиться также в. Неорганические анионы, содержащие серу, часто играют важную роль как ли / гаяды при образовании комплексов с относительно низкой устойчивостью; тем Hie менее тио-цианатные и тиосульфатные комплексы имеют большое значение для анализа. Содержащие серу соединения можно разложить ( восстановлением или гидрированием с образованием сероводорода. Оба способа применимы для надежного определения серы. Например, весьма чувствительный и избирательный метод обнаружения и определения сероводорода основан на синтезе метилено-вого синего. [43]
Специальными опытами установлено, что в растворах аммиака без тиосульфата золото не растворяется даже при 200 С, а серебро растворяется уже при 60 - 80 С, особенно если к аммиачному раствору добавить сульфат аммония или соли меди. Иными словами, основным процессом, определяющим переход золота в раствор при автоклавном аммиачном выщелачивании сульфидных концентратов, является образование не аммиачных, а тиосульфатных комплексов золота. На некоторых особенностях этого процесса необходимо остановиться более подробно. [44]
С углеродом медь и ее аналоги непосредственно не соединяются. Однако карбиды Си, Ag и Аи могут быть получены косвенным путем - действием ацетилена на аммиачные растворы с олей Си и Ag или на раствор тиосульфатного комплекса Аи Образующиеся карбиды ( точнее, ацетилиды) - коричнево-красный СигС2, белый AgjCj и желтый Аи2С2 - в воде практически нерастворимы и в сухом состоянии чрезвычайно взрывчаты. [45]
Страницы: 1 2 3 4