Я-аллильный комплекс
Cтраница 2
Таким путем образуется новый я-аллильный комплекс. Если R отличается от R, стереохимический результат реакции с участием этого комплекса может быть иным. Из этого становится понятным тот факт, что при реакции сдваивания, согласно данным Кори [65, 68], часто получается смесь стереоизомеров. Подбор соответствующих заместителей и подходящих растворителей дает, однако, возможность осуществить стереоселективную реакцию л-аллильной группы для большого числа соединений с различными типами заместителей. [16]
Нами изучены гидрогенолиз я-аллильных комплексов никеля ( бис-л-аллил ( кротил) никельхлорида) и каталитическое гидрирование с его участием. [17]
Катализаторы на основе я-аллильных комплексов переходных металлов в ряде случаев обеспечивают высокую стореоспецифичпость. [18]
В этом методе синтеза я-аллильных комплексов применяются циклические и открытые моноолефины, имеющие хотя бы одно незамещенное а-положе-ние. [19]
Имеется довольно большой ряд я-аллильных комплексов, состав которых не позволяет отнести их ни к одному из перечисленных выше классов, хотя многие из них получены из этих основных типов в результате обсуждавшихся реакций замены лигандов. В отдельных случаях они образуются совсем особыми путями. Так, аллильные производные аниона пента ( циано) кобальтата [ C3H5Co ( CN) 5 ] 3 - [539] получаются при рбработке цианокобальтатов бромистым аллилом и содержат о-аллильную группу. [20]
Таким образом, участие я-аллильного комплекса в процессе карбонилирования и переход его в ст-ацильный комплекс на одной из промежуточных стадий подтверждаются разными методами. [21]
Это обусловлено большей стабильностью я-аллильных комплексов по сравнению с а-аллильными. [22]
Таким образом, реакции я-аллильных комплексов виниллактона на никелевых комплексах приводят к образованию линейных продуктов. Поведение координированной группы может быть совершенно иным, если проводить реакцию в другой среде или на других металлах. Например, координированная на палладии кротильная группа дает неразветвленные продукты в реакции карбонилирования, однако в недавно описанных реакциях внедрения бутадиена и окиси углерода [73] взаимодействие осуществляется по внутреннему атому углерода аллильной группы. [23]
 |
Симметричная сэндви-чевая структура ферроцена. [24] |
Соединения этого типа называют я-аллильными комплексами. [25]
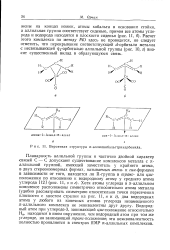 |
Вероятная структура я-аллилкобальттрикарбонила. [26] |
Хотя атомы углерода в я-аллильном комплексе расположены симметрично относительно атома металла ( удобно рассматривать симметрию относительно точки пересечения плоскости с хвостом стрелки на рис. 11, в и г), два водородных атома у любого из конечных атомов углерода незамещенного я-аллильного комплекса не эквивалентны друг другу. Водородный атом при углероде-3, занимающий цыс-положение относительно На, находится в ином окружении, чем водородный атом при том же углероде, но занимающий mpowc - положение; эта неэквивалентность полностью проявляется в спектрах ЯМР я-аллильных комплексов. [27]
Найдено, что превращение в я-аллильные комплексы определяется размером циклоолефинового кольца. Так, я-комплекс [ Р ( Цциклогептен) С12 ] 2 при нагревании в уксусной кислоте очень легко отщепляет НС1, образуя соответствующий я-циклогептенильный комплекс. [28]
В случае диенов они образуют я-аллильные комплексы, которые могут привести к образованию димерных продуктов. [29]
Описаны попытки электрофильного замещения у я-аллильных комплексов на примере C3H6Fe ( CO) 3X [165] и C3H5PdC5H5 [644] - - ацилирование, металлирование, меркурирование и др. Попытки эти имели отрицательный результат. [30]
Страницы: 1 2 3 4