Арре-ниус
Cтраница 2
Экспериментальные точки удовлетворительно описываются законом Арре-ниуса. Прямые имеют одинаковый наклон, отвечающий энергии активации 13 ккал / молъ. [16]
Теория электролитической диссоциации, созданная Арре-ниусом в 80 - х годах прошлого века, находится в полном согласии с экспериментальными данными, полученными Раулем, а до него Рюдорффом и де Коппе. [17]
Одним из важнейших критериев правильности теории Арре-ниуса является совпадение значений степени диссоциации, найденных различными методами. В случае сильных электролитов достаточное совпадение наблюдается лишь при крайних разбавлениях, когда а близка к единице. В остальных случаях наблюдаются расхождения, значительно превышающие ошибки измерений, причем величина расхождения увеличивается с валентностью ионов. Данные, полученные из криоскопических измерений ( ак), и данные по электрической проводимости ( ах) существенно расходятся, что можно иллюстрировать следующим образом. [18]
Энергию активации можно вычислить но уравнению Арре-ниуса, если известны, по крайней мере, две константы скорости при двух температурах. Энтропия активации рассчитывается по известной энергии активации процесса и температурной зависимости константы скорости реакции. [19]
С точки зрения теории электролитической диссоциации Арре-ниуса, кислотами стали называть электролиты, диссоциирующие в водных растворах с образованием ионов водорода; основаниями - электролиты, образующие в водных растворах ионы гидроксила. Взаимодействие ионов водорода с ионами гидроксила, приводящее к образованию молекул воды, начали называть реакцией нейтрализации. [20]
Во-первых, скорость гидрирования следует уравнению Арре-ниуса без каких-либо аномалий. Бензол может даже находиться в контакте с никелем Ренея при температурах свыше 250 С без каких-либо последствий. В то же время в присутствии даже менее активных катализаторов, но в газовой фазе бензол дает углеродистые отложения наряду с выделением метана. [21]
С точки зрения теории электролитической диссоциации Арре-ниуса, кислотами стали называть электролиты, диссоциирующие в водных растворах с образованием ионов водорода; основаниями - электролиты, образующие в водных растворах ионы гидроксила. Взаимодействие ионов водорода с ионами гидроксила, приводящее к образованию молекул воды, начали называть реакцией нейтрализации. [22]
Оствальд оставался до конца жизни другом Арре-ниуса, заботился об его научном росте, широко пропагандировал его теорию в таких своих классических работах, как Учебник общей химии ( 1883 - 1887), Научные основы аналитической химии ( 1894), Электрохимия, ее история и теории ( 1896) и других. [23]
Сама по себе существенная нелинейность закона Арре-ниуса характерна для кинетики химических реакций; от нее нельзя избавиться, и именно поэтому в теории неизотермических реакций получено так мало аналитических результатов. [24]
Для того чтобы описать максимум на кривой Арре-ниуса, которая отвечает экспоненциальному увеличению скорости окисления, нужно ввести два различных типа реакционных мест. [25]
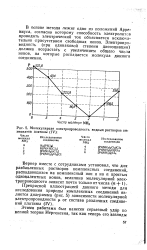 |
Молекулярная электропроводность водных растворов аммиакатов платины ( IV. [26] |
В основе метода лежит одно из положений Арре-ниуса, согласно которому способность электролитов проводить электрический ток объясняется исключительно Присутствием свободных ионов. [27]
 |
Изменение содержания кристаллизационной воды в продукте при обезвоживании растворов хлорида магния. [28] |
Общий вид уравнения близок к известному уравнению Арре-ниуса. [29]
Если прямая и обратная реакции подчиняются уравнению Арре-ниуса и энергии активации Аг Aat или реакции следуют другим более сложным зависимостям со значениями температурных коэфициен-тов, большими единицы, и k t - k t, что обычно наблюдается при экзотермических процессах, скорости обеих реакций при повышении температуры будут также расти, но в разной степени каждая. [30]
Страницы: 1 2 3 4