Арре-ниус
Cтраница 3
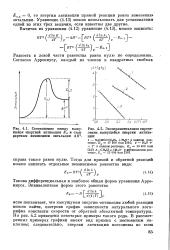 |
Соотношение между кажущейся энергией активации. а и стандартным изменением энтальпии АН9.| Экспериментальное определение, кажущейся энергии активации. [31] |
Такова дифференциальная и наиболее общая форма уравнения Арре-ниуса. [32]
Однако физический смысл этой зависимости был вскрыт Арре-ниусом [416] в 1889 г., который дал ей правильное истолкование на основе кинетической теории. [33]
Скорость пламени зависит от температуры горения по закону Арре-ниуса с теплотой активации, равной одной четверти суммы энергии активации рождения цепей и энергии активации реакции продолжения цепи. Этот результат был получен впервые Сполдингом [1 ] с привлечением специальной гипотезы, согласно которой состав реагирующего газа и, в частности, концентрация активных центров, при данной температуре в пламени принимались такими же, как и в гомогенной реакционной зоне. [34]
Статистическая теория кинетических процессов, основанная на гипотезе Арре-ниуса о переходном состоянии, была успешно разработана Эйрингом и сотрудниками [ G85 ] и применена к явлениям диффузии в конденсированных фазах. [35]
 |
Зависимость выхода метилового спирта от температуры реакции при среднем диаметре зерен катализатора 0 38 мм, 250 атм, На. СО 8, 450000 ч - 1. [36] |
Температурная зависимость константы скорости прямой реакции описывается уравнением Арре-ниуса и соответствует энергии активации Е 24 кк. [37]
На рубеже XIX и XX столетий шведский ученый Сванте Арре-ниус ( в 20 - е гг. XX столетия он был избран иностранным почетным членом Академии наук СССР) показал важнейшую роль углекислого газа и паров воды в тепловом режиме атмосферы. Проведенные впоследствии расчеты показали, что увеличение количества углекислого газа в атмосфере в 2 - 3 раза способно повысить температуру приземных слоев воздуха на 8 - 9 С, а его уменьшение на 40 % снизит среднюю глобальную температуру на 4 - 5 С. [38]
Этот факт не мог быть объяснен теорией электролитической диссоциации Арре-ниуса, поскольку с уменьшением концентрации электролита должно было происходить увеличение степени диссоциации и, следовательно, изменение спектров поглощения. Полная диссоциация сильного электролита объясняла постоянство молярных коэффициентов поглощения, поскольку при всех концентрациях раствора светопоглощаю-щими частицами оставались одни и те же ионы. Аналогичный характер имеет концентрационная зависимость вращения плоскости поляризации и ряда других свойств растворов сильных электролитов. [39]
Можно заметить, что предположения, основывающиеся на уравнении Арре-ниуса, оправдываются. [40]
Этот факт не мог быть объяснен теорией электролитической диссоциации Арре-ниуса, поскольку с уменьшением концентрации электролита должно было происходить увеличение степени диссоциации и, следовательно, изменение спектров поглощения. Полная диссоциация сильного электролита объясняла постоянство молярных коэффициентов поглощения, поскольку при всех концентрациях раствора светопоглощаю-щими частицами оставались одни и те же ионы. Аналогичный характер имеет концентрационная зависимость вращения плоскости поляризации и ряда других свойств растворов сильных электролитов. Теория электролитической диссоциации не может объяснить постоянство теплот нейтрализации хлорной, соляной и других сильных кислот гидроксидами щелочных металлов. [41]
Таким образом, в настоящее время представления Оствальда - Арре-ниуса о катализе прототропных превращений ионами водорода и гид-роксил-ионами должны быть заменены представлениями о катализе прототропных превращений кислотами и основаниями в обобщенном смысле. [42]
Полученные данные ( рис. 1) подтверждают применимость уравнения Арре-ниуса для данной реакции. [43]
Для разбавленных растворов слабых электролитов, для которых теория диссоциации Арре-ниуса приложима, можно получить эффективную концентрацию с небольшой ошибкой, умножая моляраую концентрацию на степень диссоциации. [44]
Энергию активации, как обычно, можно определить из графика Арре-ниуса по температурной зависимости константы скорости. [45]
Страницы: 1 2 3 4