Хлоридный комплекс
Cтраница 2
Хлоридный комплекс этиленпалла-дия ( C2H4PdCl2) 2 при 5 взаимодействует с изопропанолом, давая через 4 час винилизопропиловый эфир ( выход 1 6 мол. [16]
Хлоридные комплексы галлия [ GaCl4) - образуют с родамином Б ( см. стр. [17]
Хлоридный комплекс четырехвалентного селена при этом полностью остается в водной фазе. Таким путем удается легко отделять любые количества теллура от селена. [18]
Фторидные и хлоридные комплексы поглощают свет главным-образом в ультрафиолетовой области. Циглер [1363] показал возможность фотометрического определения ( при 512 нм) родия в виде комплекса RhCl3 - OSe gHg ( с дифе-нилселеноксидом), экстрагирующегося метиленхлоридом; закон Вера соблюдается при концентрации родия в экстракте 0 01 - 0 15 мкг / мл. [19]
Хлоридные комплексы двухвалентной меди легко определить по зеленому цвету, которым они обладают в концентрированных растворах соляной кислоты. Ион СиС13 ( Н20) - обычно записывают в виде CuClg; весьма вероятно, что в состав иона входит молекула воды, указанная в первой формуле. И действительно, ион Си ( НгО) 3С1 также существует в растворе, что можно утверждать с большой степенью вероятности. [20]
Хлоридные комплексы двухвалентной меди легко определить по зеленому цвету, который они имеют в концентрированных растворах соляной кислоты. Ион СиС13 ( Н20) - обычно записывают в виде CuCla; весьма вероятно, что в состав иона входит молекула воды, указанная в первой формуле. И действительно, ион Си ( Н20) 3С1 также существует в растворе, что можно утверждать с большой степ пью вероятности. [21]
Хлоридный комплекс четырехвалентного селена при этом полностью остается в водной фазе. Таким путем удается легко отделять любые количества теллура от селена. [22]
Экстракция хлоридных комплексов используется значительно чаще, чем извлечение других галогенидных или псевдогалоге-нидных комплексов. Связано это прежде всего с доступностью и распространенностью соляной кислоты. Экстракция из такого рода смесей в ряде случаев имеет преимущества. Одно из них - экономия дефицитной соляной кислоты при промышленном использовании экстракции - применение смеси дешевых NaCl и H2S04 оказывается гораздо более экономичным. Коэффициенты распределения металлов иногда резко возрастают при замене соляной кислоты на хлорид лития, особенно при общей высокой концентрации хлорид-иона; примером может служить экстракция Со, Мп ( П) или Си трибутилфосфатом. Экстракция хлоридных комплексов имеет большое практическое значение; ее широко применяют в аналитической химии и радиохимии, начинают использовать в гидрометаллургии. [23]
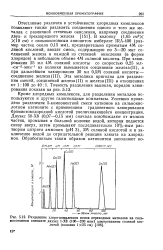 |
Разделение хлоро-комплексов ионов переходных металлов на сильноосновном анионите дауэкс 1 - Х8 ( 100 - 200 мкм элюированием соляной кислотой ( колонки 1X25 см. [24] |
Кроме хлоридных комплексов, для разделения металлов используются и другие галогенидные комплексы. Успешно проведено разделение 5-компонентной смеси катионов на сильнокислотном катионите с применением градиентного элюирования бромистоводородной кислотой увеличивающейся концентрации. Дауэкс 50 - Х8 ( 0 07 - 0 15 мм) сначала освобождают от мелких частиц, промывая в большой колонке водой, которая подается снизу вверх, затем промывают последовательно 10 % - ным раствором цитрата аммония ( рН 3), ЗМ соляной кислотой и в заключение водой до отрицательной реакции элюата на хлорид-ион. [25]
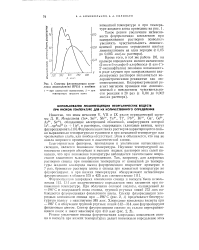 |
Спектры флуоресценции комплекса люмогаллиона ИРЕА с ниобием. [26] |
Флуоресценция хлоридных комплексов свинца и висмута была использована 112, 13 ] для количественного определения этих элементов при пониженной температуре. При облучении соляной кислоты, охлажденной до - 196 С и содержащей ионы свинца, группой ртутных линий 272 ммк наблюдается флуоресценция фиолетового цвета. Спектр флуоресценции хлоридных комплексов свинца при - 196 С ( рис. 2, 1) представляет бесструктурную полосу с максимумом 385 ммк. Хлоридные комплексы висмута при - 196 С и облучении группой ртутных линий 312 - 314 ммк флуоресцируют фиолетовым цветом. [27]
Роль хлоридных комплексов макрокомпонентов весьма существенна при загрязнении грунтовых вод попутными водами нефтедобычи и сточными водами добычи и переработки галургического сырья, относящимися к хлоридному типу. В регионах развития глиноземно-алюминиевой промышленности в процессе полной техногенной метаморфизации грунтовых вод происходит накопление карбонатных комплексов макрокомпонентов. [28]
У хлоридных комплексов Pb и иодид-ных комплексов Т1 при размораживании растворов от-196 до 0 С наблюдается резкое изменение цвета люминесценции от синего к зеленому. [30]
Страницы: 1 2 3 4